微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、计算题 PM2.5(可入肺颗粒物)污染跟冬季燃煤密切相关,燃煤还同时排放大量的CO2、SO2和NOx
(1)最近有科学家提出构想:把空气吹入饱和碳酸钾溶液,然后再把CO2从溶液中提取出来,经化学反应后使之变为可再生燃料甲醇。
①已知在常温常压下:
2CH3OH(l)+3O2(g) = 2CO2(g)+4H2O(g)??H = -1275.6 kJ/mol
2CO(g)+O2(g)=2CO2(g)???H = -566.0 kJ/mol?????
H2O(g)=H2O(1)??H = -44.0 kJ/mol
则甲醇不完全燃烧生成一氧化碳和液态水的热化学方程式为_____________________。
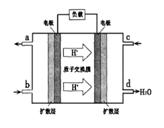
②以甲醇和氧气反应制成的燃料电池如图所示,该电池工作过程中O2应从______(填“c”或“b”)口通入,电池负极反应式为__________________。
③25℃时,将甲醇燃烧生成的足量CO2通入到浓度为0.lmol・L-1,NaOH溶液中,所得溶液的pH=8,溶液中离子浓度由大到小的顺序是_________________。
(2)已知在一定条件下,NO与NO2存在下列反应:NO(g)+NO2(g)=N2O3(g),ΔH<0若该反应在绝热、恒容的密闭体系中进行,下列示意图能说明tl时刻达到平衡状态的是____________。

(3)在一个固定容积为5L的密闭容器中充入0.20molSO2和0.l0molO2,半分钟后达到平衡,测得容器中含SO30.18mol,则v(O2)=__________,若继续通入0.20mo1SO2和0.lmolO2,则平衡____________移动(填“向正反应方向”、“向逆反应方向”或“不”)。
(4)在一定条件下,NO2可以被NH3还原为N2来消除NO2对环境造成的污染。25℃时,将NH3溶于水得l00mL 0.lmol・L-的氨水,测得pH=11,则该条件下NH3・H2O的电离平衡常数约为___________。
参考答案:(16分)
(1)?①CH3OH(l)+O2(g)=
本题解析:
试题分析:
(1)①根据盖斯定律①-②-③×4得到CH3OH(l)+O2(g)=CO(g)+2H2O(l)?△H=-442.8kJ・mol-1。②结合图像电池中质子移向正极,O2在正极反应。应从c通入,发生O2+4e-+4H+=2H2O,所以负极为CH3OH+ H2O-6e-=CO2↑+6H+。③溶液的pH=8应为溶质为碳酸氢钠,离子浓度由大到小的顺序是c(Na+)> c(HCO- 3)> c(OH-)> c(H+)> c(CO2- 3)。
(2)达到平衡状态
本题难度:一般
2、选择题 下列说法中正确的是
A.将NaHSO4晶体加热熔融时有两种化学键断裂
B.水分子间因为存在氢键,所以加热至较高温度时也难以分解
C.根据金属晶体的共性可知金属键和离子键一样没有方向性和饱和性
D.以极性共价键形成的分子一定是极性分子
参考答案:C
本题解析:A:加热熔融时,NaHSO4=Na+ + HSO4―,很明显只有离子键断裂;
B:水的稳定性决定于分子内的H―O键的稳定性,与氢键无关
C:正确;
D:例如CH4即是以极性键组成的非极性分子,键的极性与分子极性不能混淆。
本题难度:一般
3、选择题 下列物质的变化中,有共价键明显被破坏的是( )
A.I2升华
B.NaCl颗粒被粉碎
C.酒精溶于水得到酒精溶液
D.从NH4HCO3中闻到了刺激性气味
参考答案:A、碘的升华是物理变化,只是物质状态的变化,共价键没被破坏,
本题解析:
本题难度:一般
4、选择题 下列物质中,既含有离子键,又含有共价键的是(?)
A.H2O
B.NaOH
C.CaCl2
D.H2SO4
参考答案:B
本题解析:考查化学键的判断。一般活泼的金属和活泼的非金属容易形成离子键,非金属元素的原子间容易形成共价键。所以选项A~D中的化学键分别为极性键、离子键和极性键、离子键、极性键。因此答案选B。
本题难度:一般
5、选择题 下列叙述错误的是( )
A.原子间通过共用电子对形成的化学键叫共价键
B.阴、阳离子之间通过静电作用形成的化学键叫做离子键
C.化学键是相邻的原子之间强烈的相互作用
D.化学键是既存在于相邻原子间,也存在于相邻分子间的相互作用
参考答案:A.原子之间通过共用电子对形成的化学键为共价键,故A正确;<
本题解析:
本题难度:一般