微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 对于反应4Fe(OH)2(s) +2H2O(l)+O2(g)= 4Fe(OH)3(s) △H=-444.3kJ・mol-1,且熵减小,在常温常压下该反应能自发进行,对反应的方向起决定作用的是
[???? ]
A.焓变
B.温度
C.压强
D.熵变
2、选择题 将一定量纯净的氨基甲酸铵置于特制的密闭真空容器中(假设容器体积不变,固体试样体积忽略不计),使其达到分解平衡:NH2COONH4(s) 2NH3(g)+CO2(g)。实验测得不同温度下的平衡数据列于下表:
2NH3(g)+CO2(g)。实验测得不同温度下的平衡数据列于下表:
温度/℃
| 15.0
| 20.0
| 25.0
| 30.0
| 35.0
|
平衡总压强/kPa
| 5.7
| 8.3
| 12.0
| 17.1
| 24.0
|
平衡气体总浓度/10-3mol/L
| 2.4
| 3.4
| 4.8
| 6.8
| 9.4
A 该可逆反应达到平衡的标志之一是混合气体平均相对分子质量不变
B 因该反应熵变(△S)大于0,焓变(△H)大于0,所以在低温下自发进行
C根据表中数据,计算15.0℃时的分解平衡常数约为2.0×10-9(mol・L-1)3
D达到平衡后,若在恒温下压缩容器体积,氨基甲酸铵固体的质量减小
3、填空题 在一个容积固定不变的密闭容器中进行反应:2A(g)+B(g)==3C(g)+D(s),已知将2molA和1molB充入该容器中,反应在某温度下达到平衡时,C的物质的量为Wmol,C在平衡混合气体中的体积分数为n%。
⑴可认定上述可逆反应在一定条件下已达到化学平衡状态的是???????(选填序号)。
A、体系压强不再变化?????????????????? B、v正(A)=2v逆(B)
C、体系的密度不再变化???????????????? D、混合气体的平均相对分子质量不再变化
⑵如果用下列情况的配比作起始物,在同样的容器和温度下达到平衡,其结果一定是:
C的物质的量为2Wmol,C在平衡混合气体中的体积分数仍为n%的是??????????
A、4molA+2molB?????????????????????? B、6molC+1molD
C、1molA+0.5molB+1.5molC+0.5molD???? D、2molA+1molB+3molC+1molD
E、2molA+1molB+3molC+2molD
⑶若维持该题条件不变,仅从生成物开始配比,要求达到平衡时,C的物质的量仍为Wmol,则D的起始物质的量n(D)应满足的条件是???????(用含W的代数式表示)
⑷此反应的v―t图象如甲图,若其他条件都不变,只是在反应前加入合适的催化剂,则
其v―t图象如乙图,请用“=、<、>”填空:①a1????a2;②b1?????b2;③两图中
阴影部分面积:甲????乙。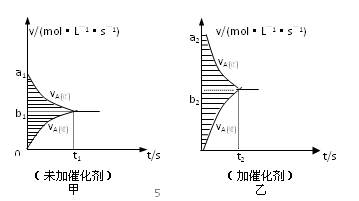
4、选择题 下列有关说法正确的是
A.因为合金在潮湿的空气中易形成原电池,所以合金耐腐蚀性都较差
B.常温下,MgO(s)+C(s)=Mg(s)+CO(g)不能自发进行,则其△H>0
C.在NaCl和KBr的混合溶液中滴加AgNO3溶液,一定先产生淡黄色沉淀
D.加热0.1 mol・L-1Al2(SO4)3溶液,水解程度增大、溶液的酸性增强
5、选择题 下列说法正确的是[???? ]
A.食物在常温下腐败是自发进行的
B.凡是放热反应都是自发的
C.自发反应都是熵增大的反应
D.电解池的反应是属于自发反应
|