微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 已知某温度下,四种一元弱酸的电离平衡常数为:Ka(HCN)=6.2×10-10mol/L、Ka(HF)=6.8×10-4mol/L、Ka(CH3COOH)=1.8×10-5mol/L、Ka(HNO2)=6.4×10-6mol/L。物质的量浓度都为0.1 mol/L的下列溶液中,pH最小的是(???)
A.HCN
B.CH3COOH
C.HF
D.HNO2
参考答案:C
本题解析:
试题分析:电离平衡常数类似于化学平衡常熟,平衡常数越大,电离程度越大。因此根据平衡常数大小可以判断四种一元酸的相对强弱,即HF的酸性最强,所以在浓度相等的条件下,HF的酸性最强,pH最小,答案选C。
点评:对于一元弱酸,电离平衡常数越大,酸性越强,据此可以判断。
本题难度:一般
2、填空题 (15分)某食用白醋是由醋酸与纯水配制而成,用中和滴定的方法准确测定其中醋酸的物质的量浓度。实验步骤:①配制500mL浓度约为0.1 mol・L-1的NaOH溶液;②用物质X的标准溶液准确测定该NaOH溶液的浓度(X与氢氧化钠按物质的量比1:1完全反应);③用已知准确浓度的NaOH溶液测定醋酸的浓度。
(1)称量所需的NaOH固体置于大烧杯中,加入500mL蒸馏水,搅拌溶解。该配制步骤__________(填“可行”或“不可行”)。
(2)称量时NaOH在空气中极易吸水,配制所得的NaOH溶液浓度通常比预期_____(填“小”或“大”),这是不能直接配制其标准溶液的原因。
(3)查阅白醋包装说明,醋酸含量约为6g/100mL,换算成物质的量浓度约为_____ mol・L-1,滴定前将白醋稀释_________(填“10”或“100”)倍。(已知醋酸的相对分子质量为60)
(4)稀释白醋时需要的仪器有烧杯、玻璃棒、滴管、酸式滴定管、___________。
(5)准确量取稀释后的白醋20.00mL,置于250mL锥形瓶中,加水30mL,再滴加酚酞指示剂,用上述NaOH标准溶液滴定至____________即为终点。重复滴定两次,平均消耗NaOH标准溶液V mL(NaOH溶液浓度为c mol・L-1)。
(6)原白醋中醋酸的物质的量浓度=____________ mol・L-1。
参考答案:(1)可行(2分)??(2)小(2分)????(3)1 (2
本题解析:(1)根据题意可知,氢氧化钠的浓度不需要准确配制,所以不需要容量瓶,因此是可行的。
(2)氢氧化钠易吸水,导致称量的氢氧化钠固体质量偏小,浓度偏低。
(3)6g乙酸是0.1mol,所以浓度是0.1mol÷0.1L=1.0mol/L。浓度太高反应太快,不利于判断终点,太低,反应太慢,所以稀释10倍即可。
(4)应用醋酸的浓度需要是准确的,因此应该用容量瓶配制。
(5)酸不能使酚酞试液显色,碱能使酚酞试液显红色,所以终点时的现象是溶液变成浅红色且30秒内不褪色。
(6)根据氢离子
本题难度:一般
3、选择题 向浓度为1 mol/L的FeCl2溶液中通入足量的Cl2。下列有关溶液中离子浓度大小关系一定错误的是
A.原FeCl2溶液中:c(Cl-) > c(Fe2+) > c(H+) > c(OH-)
B.原FeCl2溶液中:2c(Fe2+) + c(H+) = c(Cl-) + c(OH-)
C.反应后的溶液中:c(Fe3+) > c(Cl-) > c(H+) > c(OH-)
D.反应后的溶液中:3c(Fe3+) + c(H+) = c(Cl-) + c(OH-)
参考答案:C
本题解析:原溶液被氯气氧化:2FeCl2+Cl2=2FeCl3,得到FeCl3溶液
FeCl2溶液中电荷守恒为:2c(Fe2+) + c(H+) = c(Cl-) + c(OH-),B正确
由于Fe2+部分水解,溶液呈酸性,故c(Cl-) > c(Fe2+) > c(H+) > c(OH-),A正确
FeCl3溶液中电荷守恒为:3c(Fe3+) + c(H+) = c(Cl-) + c(OH-) ,D正确
由于Fe3+部分水解,溶液呈酸性,故c(Cl-) > c(Fe
本题难度:一般
4、选择题 今有两种正盐的稀溶液,分别是a mol/LNaX溶液和b mol/LNaY溶液,下列说法不正确的是??????????( ???)
A.若a=b,且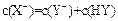 ,则相同条件时,酸性
,则相同条件时,酸性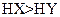
B.若a=b,且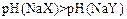 ,则相同条件时,酸性
,则相同条件时,酸性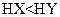
C.若a>b,且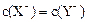 ,则相同条件时,酸性HX<HY
,则相同条件时,酸性HX<HY
D.若等体积混合,且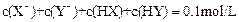 ,则一定有
,则一定有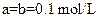
参考答案:D
本题解析:略
本题难度:一般
5、选择题 反应:H2S(g)+aO2(g)
参考答案:
本题解析:
本题难度:一般