微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 已知NaHSO3溶液显酸性,溶液中存在以下平衡:
HSO3-+ H2O  ?H2SO3 + OH-????①
?H2SO3 + OH-????①
HSO3- ?H+ + SO32-????????????②
?H+ + SO32-????????????②
向0.1mol・L-1的NaHSO3溶液中分别加入以下物质,下列有关说法正确的是
A.加入少量金属Na,平衡①左移,平衡②右移,溶液中c(HSO3-)增大
B.加入少量Na2SO3固体,则c(H+) + c(Na+) = c(HSO3-) + c(OH-) +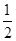 c(SO32-)
c(SO32-)
C.加入少量NaOH溶液, 、
、 的值均增大
的值均增大
D.加入氨水至中性,则2c(Na+) = c(SO32-)>c(H+) = c(OH-)
参考答案:C
本题解析:NaHSO3溶液显酸性,说明HSO3-的电离程度大于其水解。A、加入的Na与水反应生成NaOH,与HSO3-反应,故c(HSO3-)减小,错误;B、该溶液中存在电荷守恒,故c(SO32-)前的系数为2,错误;C、加入少量NaOH,c(SO32-)增大,c(HSO3-)减小,c(OH-)增大,c(H+)减小,故正确;D、c(Na+)=2c(SO32-),错误。
【考点定位】考查电解质溶液,涉及弱电解质的电离和盐类的水解、三大守恒关系的应用。
本题难度:一般
2、选择题 已知在硝酸溶液中加入铝粉不产生氢气.若在加入铝粉能放出氢气的无色溶液中,分别加入下列各组离子,可能大量共存的是( )
A.Ca2+、NO3ˉ、CO32-、Na+
B.Na+、Ba2+、Mg2+、HCO3-
C.NO3ˉ、Cu2+、K+、Clˉ
D.NO3ˉ、K+、AlO2ˉ、OHˉ
参考答案:与铝反应产生大量氢气的溶液可能是酸溶液,也可能是碱溶液,
本题解析:
本题难度:简单
3、选择题 离子间能大量共存,当溶液中c(H+)=10-1mol?L-1时有气体产生,而当溶液中c(H+)=10-13mol?L-1时又能产生沉淀.下列各组离子中符合上述要求的一组是( )
A.Ba2+K+CO32-Cl-
B.Na+K+NO3-CO32-
C.Mg2+NH4+SO32-Cl-
D.Fe2+Na+SO32-NO3-
参考答案:A.因Ba2+、CO32-能结合生成沉淀,则不能共存,故A不
本题解析:
本题难度:一般
4、选择题 在溶液中加入足量的Na2O2后仍能大量共存的是 ( )
A.NH4+、NO3-、Ba2+、Cl-
B.K+、SO42-、Cl-、AlO2-
C.NO3-、HCO3-、Ca2+、Mg2+
D.Cl-、Na+、CO32-、SO32-
参考答案:B
本题解析:
试题分析:由题可知道,加入Na2O2后,生成了NaOH,并且Na2O2有氧化性,能氧化一些还原性物质,对于A选项,NH4+与OH-生成了NH3.H2O;C选项中HCO3-、Ca2+、Mg2+与OH-不能大量共存;D选项中,SO32-具有还原性,被氧化了,只有B符合要求。
考点:离子的共存问题
点评:该题是基础性试题的考查,属于高考中的常见考点之一,该题有一定的难度,特别容易错选D。
本题难度:简单
5、选择题 下列各组中的离子,能在溶液中大量共存的是
A.Ba2+、Na+、Cl-、SO42-
B.Ag+ 、Al3+ 、NO3- 、H+
C.Na+、HCO3-、Cl-、OH-
D.K+ 、H+ 、SO42-、OH-
参考答案:B
本题解析:
试题分析:A、Ba2+和SO42-不能大量共存,错误;B、离子可以大量共存,正确;C、碳酸氢根离子和氢氧根离子不能大量共存,错误;D、氢离子和氢氧根离子不能大量共存,错误。
本题难度:一般