微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、实验题 (6分)I.有关中和滴定的操作有:①用标准溶液润洗滴定管??②往滴定管内注入标准溶液?③检查滴定管是否漏水?④滴定?⑤洗涤
正确的操作顺序是??????????(填字母)
A.⑤①②③④
B.③⑤①②④
C.⑤②③①④
D.②①③⑤④
Ⅱ.氧化还原滴定实验同中和滴定类似(用已知浓度的氧化剂溶液滴定未知浓度的还原剂溶液或反之)。现有0.001mol・L-1KMnO4酸性溶液和未知浓度的无色NaHSO3溶液。反应的离子方程式是:2MnO4-+5HSO3-+H+= 2Mn2++5SO42-+3H2O
填空回答下列问题:
(1)不用????????(填“酸式”或“碱式”)滴定管盛放高锰酸钾溶液。
(2)选何种指示剂????????。(填序号)
①甲基橙????②酚酞??③石蕊???④不用指示剂
(3)滴定前平视KMnO4液面,刻度为a mL,滴定后俯视液面刻度为b mL,则
(b-a)mL比实际消耗KMnO4溶液体积???????(填“多”或“少”)。根据(b-a)mL计算得到的待测液浓度,比实际浓度???????(填“大”或“小”)。
(4)无论是KMnO4溶液往NaHSO3溶液中滴,还是NaHSO3溶液往KMnO4溶液中滴,在其他操作正确规范的前提下,下列操作一定会使测定结果偏高的是?????????。(填序号)
①取用NaHSO3溶液的滴定管未用待测NaHSO3溶液润洗
②取用KMnO4酸性溶液的滴定管未用标准KMnO4酸性溶液润洗
③滴定过程中不慎有液体溅出
④滴定前仰视读数,滴定后平视读数
参考答案:(6分)I? B??Ⅱ(1)碱式(2)④(3)少?小(4)②
本题解析:略
本题难度:一般
2、选择题 下列有关实验操作不正确的是( )
A.实验中取用的钠的剩余部分可以放回原试剂瓶中
B.做焰色反应时铂丝应用稀盐酸洗净,并灼烧至无色
C.用容量瓶配制溶液定容时加水超过刻度线,应用胶头滴管将多余的吸出
D.用浓硫酸配制一定物质的量浓度的稀硫酸时,浓硫酸溶于水后,应冷却至室温才能转移到容量瓶中
参考答案:A.实验后,将剩余药品放回原试剂瓶会污染瓶中药品,要放在指定
本题解析:
本题难度:一般
3、选择题 某同学实际配制的NaOH溶液的浓度偏低,其原因不正确的是
A.使用滤纸称量NaOH固体
B.容量瓶中原来存在少量蒸馏水
C.溶解后的烧杯未经洗涤
D.定容时仰视刻度线
参考答案:B
本题解析:
答案:B
B、容量瓶中原来存在少量蒸馏水,不影响配制结果。A、NaOH固体吸水C.溶解后的烧杯未经洗涤,两者均使溶质减少;D定容时仰视刻度线,加水偏多,实际配制的NaOH溶液的浓度偏低。
本题难度:简单
4、选择题 下列实验能达到预期目的的是
A.向煮沸的1 mol・L-1NaOH溶液中滴加FeCl3饱和溶液制备Fe(OH)3胶体
B.向乙酸乙酯中加入饱和Na2CO3溶液,振荡,分液分离除去乙酸乙酯中的少量乙酸
C.称取19.0 g SnCl2,用100 mL蒸馏水溶解,配制1.0 mol・L-1 SnCl2溶液
D.用氢氧化铜粉末检测尿糖
参考答案:B
本题解析:Fe(OH)3胶体的制备方法是向沸水中加入几滴饱和FeCl3溶液:Fe3++3H2O(沸水)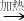 Fe(OH)3(胶体)+3H+,若NaOH溶液与FeCl3溶液混合则出现Fe(OH)3沉淀;由于2CH3COOH+Na2CO3=2CH3COONa+H2O+CO2↑,乙酸乙酯不与Na2CO3溶液反应,也不溶于水中,B正确
Fe(OH)3(胶体)+3H+,若NaOH溶液与FeCl3溶液混合则出现Fe(OH)3沉淀;由于2CH3COOH+Na2CO3=2CH3COONa+H2O+CO2↑,乙酸乙酯不与Na2CO3溶液反应,也不溶于水中,B正确
本题难度:一般
5、选择题 准确量取25.00 mL高锰酸钾溶液,可选用的仪器是
A.50 mL量筒
B.10 mL量筒
C.50 mL酸式滴定管
D.50 mL碱式滴定管
参考答案:C
本题解析:考查滴定管的结构、使用,滴定管、量筒的精确程度.本题KMnO4是强氧化剂,不能使用带有胶管的碱式滴定管.滴定管刻度精确到0.1 mL,可估读到0.01 mL,符合本题量取要求,而量筒(即使是本题的小量筒)没有这样的精确度.
本题难度:困难