微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、填空题 化学兴趣小组为探究某铁矿石(主要成分为Fe203和Si02)的性质,进行如下实验:
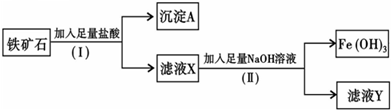
(1)步骤(I)中分离溶液和沉淀的操作名称是______;
(2)沉淀A中一定含有______,该物质属于______(填“酸性”或“碱性”)氧化物;
(3)往滤液Y中加入KSCN溶液,溶液呈______(填“黄色”或“红色”);
(4)写出步骤(Ⅱ)中生成Fe(OH)3的离子方程式______.
参考答案:(1)铁矿石的主要成分为Fe203和Si02,加入足量盐酸后
本题解析:
本题难度:一般
2、选择题 向FeI2、FeBr2的混合溶液中通入适量氯气,溶液中某些离子的物质的量变化如图所示。已知:2Fe2++Br2=2Fe3++2Br-?;2Fe3++2I-=2Fe2++I2则下列有关说法中,不正确的是(??????)
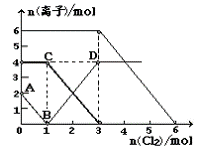
A.线段BD表示Fe3+物质的量的变化
B.原混合溶液中FeBr2的物质的量为6mol
C.当通入2molCl2时,溶液中已发生的离子反应可表示为:2Fe2++2I-+2Cl2=2Fe3++I2+4Cl-
D.原溶液中:n(Fe2+):n(I-):n(Br-)=2:1:3
参考答案:B
本题解析:略
本题难度:一般
3、选择题 由Fe2O3、Fe、CuO、C、Al中的几种物质组成的混合粉末,取样品进行下列实验(部分产物略去)。关于混合粉末的组成判断正确的是

A.一定含CuO和C???????????????????B.一定含Fe2O3、CuO和C
C.一定含CuO和C,一定不含Al???????D.气体Z为纯净物
参考答案:A
本题解析:
试题分析:能与Fe、Fe2O3、CuO、C、Al物质反应产生两种气体的浓酸不可能是浓盐酸;如果是浓硫酸,可以与C、Al、Fe单质发生氧化还原反应,浓硫酸被还原为SO2,C被氧化为CO2,Al被氧化为Al3+,铁被氧化为铁离子;如果是浓硝酸,则两种气体是CO2和NO2,其变化与加浓硫酸的反应相同.无论是那种浓酸均可以使两种氧化物Fe2O3、CuO转化为对应的盐,所以X为SO2和CO2或者CO2和NO2。向溶液X中加过量Fe粉,得Y溶液和两种固体,且一种固体为红色(Cu),另一种就是过量的Fe粉,根据
本题难度:一般
4、填空题 (6分).实验室中要除去细碎铜屑中的少量细碎铁屑,某同学设计了两个方案:
(1)Cu、Fe 过滤
过滤 洗涤
洗涤
(2)Cu、Fe 过滤
过滤 洗涤
洗涤
两个方案较好的是_______________(填序号),理由是______________________________。你是否有简便的方法,若有,请写出做法:__________________________________________。
参考答案:(2);既除去了铁,而同时又增加了铜;?用磁铁吸取铁屑
本题解析:由于在方案(2)中既除去了铁,而同时又增加了铜,而方案(1)不能使铜的质量增加,所以最后的是方案(2);由于磁铁能吸引铁,所以也可以用磁铁吸取铁屑。
本题难度:一般
5、计算题 已知:CuS、Cu2S是两种黑色不溶于水的固体,但一定条件下都能与稀HNO3反应,用离子方程式表示为:
①3CuS+8H++8NO3-=3Cu2++3SO42-+8NO↑+4H2O
②3Cu2S+16H++10NO3-=6Cu2++3SO42-+10NO↑+8H2O
现有不同质量的四份CuS、Cu2S的混合物样品分别和100mL物质的量浓度5mol/L稀硝酸充分反应,所取样品质量与产生气体体积(标准状况下测定)如下表所示:
实验序号
| a
| b
| c
|
样品质量(g)
| 9.6
| 12.8
| 64.0
|
气体体积(L)
| 5.04
| 6.72
| V
?
试回答下列问题(不考虑硝酸的挥发以及溶液体积变化):
(1)a组实验结束后,溶液中c(NO3-)=?????????;
(2)b组实验结束后,溶液的pH=???????????;
(3)通过计算分析实验c组中产生气体的体积(V)范围????????????????????。
参考答案:(1)2.75mol/L
(2) 0
(3)7L
本题解析:(1)设9.6g的样品中CuS的物质的量为x,Cu2S的物质的量为y
96x+160y=9.6?????????? 8x/3+10y/3=0.225
解得:x=y=0.0375mol, c(NO3-)= (0.5mol-0.225 mol)/0.4L=2.75mol/L
(亦可根据N原子守恒来求)
(2)设12.8g的样品中CuS的物质的量为x
本题难度:简单
|