2a-b
b
参考答案:气体体积变化(b-a)L,则:
2NH3
本题解析:
本题难度:一般
2、选择题 下列化学用语正确的是(?? )
A.CO2的电子式:
B.次氯酸的电子式: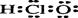
C.CH4分子的比例模型: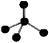
D.Cl-的结构示意图: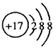
参考答案:D
本题解析:
试题分析:二氧化碳的电子式应为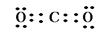 ,A错误;B项:次氯酸的电子式为 ,A错误;B项:次氯酸的电子式为 ,错误;C项表示的是甲烷的球棍模型,错误。 ,错误;C项表示的是甲烷的球棍模型,错误。
本题难度:一般
3、选择题 氢化亚铜(CuH)是一种难溶物质,用CuSO4溶液和“另一种反应物”在40℃~50℃时反应可生成它。CuH不稳定,易分解;CuH在氯气中能燃烧;跟盐酸反应能产生气体,以下有关的推断中错误的是???
A.“另一种反应物”一定具有还原性
B.CuH既可做氧化剂也可做还原剂
C.CuH+Cl2=CuCl+HCl(燃烧)
D.CuH+HCl=CuCl+H2↑(常温)
参考答案:C
本题解析:
试题分析:A、根据化合价的变化判断,CuSO4做氧化剂、所以另一物质做还原剂,一定具有还原性,正确;B、CuH中的Cu处于+1价,可升可降,所以具有氧化性也具有还原性,正确;C、,Cl2氧化性很强,能够将+1价的铜氧化,所以,生成物不可能有亚铜,不会生成CuCl,错误;D、CuH中-1价的H与HCl中+1价的H发生氧化还原反应,生成H2,正确。
本题难度:一般
4、选择题 氧化还原反应中,水的作用可以是氧化剂、还原剂、既是氧化剂又是还原剂、既非氧化剂又非还原剂等。下列反应与Br2+SO2+2H2O=H2SO4+2HBr相比较,水的作用不相同的是( )
A.2Al+2NaOH+2H2O=2NaAlO2+3H2↑
B.4Fe(OH)2+O2+2H2O=4Fe(OH)3
C.BrCl+H2O=HCl+HbrO
D.2Na2O2+2H2O=4NaOH+O2↑
参考答案:A
本题解析:
试题分析:反应Br2+SO2+2H2O=H2SO4+2HBr为氧化还原反应,水既不是氧化剂也不是还原剂,A、反应2Al+2NaOH+2H2O=2NaAlO2+3H2↑中水作氧化剂,正确;B、反应4Fe(OH)2+O2+2H2O=4Fe(OH)3中,水既不是氧化剂也不是还原剂,错误;C、反应BrCl+H2O=HCl+HBrO 不是氧化还原反应,水既不是氧化剂也不是还原剂,错误;D、反应2Na2O2+2H2O=4NaOH+O2↑中,水既不是氧化剂也不是还原剂,错误。
本题难度:一般
5、选择题 氯酸是一种强酸,氯酸的浓度超过40%,就会迅速分解,反应的化学方程式为:
8HClO3 → 3O2↑+ 2Cl2↑+ 4HClO4 + 2H2O。根据题意完成第27~30题:
27.在上述变化过程中,发生还原反应的过程是:___________→___________(填化学式)。
28.该反应的氧化产物是______________(填化学式);所得混合气体的平均式量为_______。
29.已知测定锰的一种方法是:锰离子转化为高锰酸根离子,反应体系中有H+、Mn2+、H2O、IO3―、MnO4―、IO4―离子,有关离子反应方程式为:
。
30.在锰离子转化为高锰酸根离子的反应中,如果把反应后的溶液稀释到1升,测得溶液的pH = 2,则在反应中转移电子的物质的量为 mol。
参考答案:
27.HClO3 → Cl2。(2分)
28.
本题解析:略
本题难度:困难
|