微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、简答题 某课外小组同学对不同条件下铁钉的锈蚀进行了实验.
| 实验序号 | ① | ② | ③ | ④
实验
内容

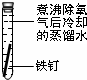

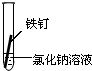
一周后观察:
(1)铁钉被腐蚀程度最大的是______(填实验序号).
(2)实验③中主要发生的是______(填“化学腐蚀”或“电化学腐蚀”).
(3)铁发生电化学腐蚀的负极反应式为:______.
(4)根据上述实验,你认为铁发生电化学腐蚀的条件是______.
(5)据资料显示,全世界每年因腐蚀而报废的金属材料相当于其年产量的20%以上.为防护金属被腐蚀可采取的措施有______(填序号).
①健身器材刷油漆??????????????????????②自行车钢圈镀铬
③将钢管用导线与镁条连接??????????????④将钢管用导线与碳棒连接.
参考答案:(1)①在干燥空气中难以腐蚀,②隔绝空气也难以腐蚀,③④发生
本题解析:
本题难度:一般
2、填空题 已知电极材料:铁.铜.银.石墨.锌.铝,电解质溶液:氯化铜溶液.硫酸铁溶液.盐酸。按要求回答下列问题:
(1)电工操作上规定:不能把铜导线和铝导线连接在一起使用,请说明原因。__________。
(2)若电极材料选铜和石墨,电解质溶液选硫酸铁溶液,外加导线构成原电池,请写出电极反应式,负极??????????????????,正极??????????????????。
(3)若总反应为:Cu+2H+= Cu2++H2,判断该装置属于原电池还是电解池?____。画出对应的装置图,标出电极材料和电解质溶液。_____
参考答案:(共7分)(1)形成原电池加速铝导线的腐蚀??????(2分
本题解析:
试题分析:(1)由于铜导线和铝导线连接在一起使用容易形成原电池,加速铝导线的腐蚀。
(2)铜是金属,石墨是非金属,则铜是负极失去电子。石墨是正极,溶液中的铁离子在正极得到电子,所以电极反应式是负极:Cu-2 e-= Cu2+;正极:2Fe3+ +2 e-=2Fe2+。
(3)铜酸反应得不到氢气,属于非自发的,所以要实现该反应,所以通过电解池。其中铜和电源的正极相连,做阳极。电解质溶液是稀硫酸,而阴极材料可以是碳棒。
点评:该题是高考中的常见题型和主要的考点,属于中等难度的试题。试
本题难度:一般
3、填空题 (16分)碘被称为“智力元素”,科学合理地补碘可防止点缺乏症。碘酸钾(KIO3)是国家规定的食盐加碘剂,它的晶体为白色,可溶于水。碘酸钾在酸性介质中与过氧化氢或碘化物作用均生成单质碘。以碘为原料,通过电解制备碘酸钾的实验装置如有图所示。
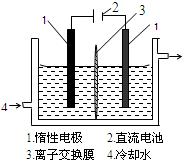
请回答下列问题:
(1)碘是___(填颜色)固体物质,实验室常用____方法来分离提纯含有少量杂质的固体碘。
(2)电解前,先将一定量的精制碘溶于过量氢氧化钾溶液,溶解时发生反应:
3I2 + 6KOH =" 5KI" + KIO3 + 3H2O,将该溶液加入阳极区。另将氢氧化钾溶液加入阴极区,电解槽用水冷却。
电解时,阳极上发生反应的电极反应式为________________________;阴极上观察到的实验现象是______________________________。
(3)电解过程中,为确定电解是否完成,需检验电解液中是否有I-。请设计一个检验电解液中是否有I-的实验方案,并按要求填写下表。
要求:所需药品只能从下列试剂中选择,实验仪器及相关用品自选。
试剂:淀粉溶液、碘化钾淀粉试纸、过氧化氢溶液、稀硫酸。
实验方法
| 实验现象及结论
| ?
| ?
(4)电解完毕,从电解液中得到碘酸钾晶体的实验过程如下:
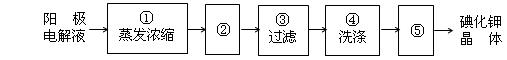
步骤②的操作名称______,步骤⑤的操作名称是____________
步骤④洗涤晶体的目的是_______________________________。
参考答案:(1) 紫黑色? (1分)???升华 (2分)
(2)
本题解析:略
本题难度:一般
4、选择题 为了防止铁腐蚀,下列做法不可取的是
A.在铁制品表面刷漆
B.将铁制品长期暴露在空气中
C.将铁制品浸在水中与空气隔绝
D.在铁制品表面镀氧化膜
参考答案:B
本题解析:铁腐蚀的必需条件为空气、水,故答案为B
本题难度:简单
5、实验题 (16分)已知金属活动相差越大,形成原电池时越容易放电。请根据如图装置,回答下列问题:
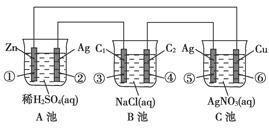
(1)各装置名称是:A池________,B池______,C池________。
(2)写出电极上发生的反应:①_____________,③___________,⑤_____________。
(3)当电路上有2 mol电子流过时,①极上质量变化______g,⑥极上质量变化______g。
(4)反应进行一段时间后,A、B、C三池中电解质溶液浓度不变的是________。
参考答案:(1)原电池 电解池 电镀池 (2)Zn-2e-===Zn2
本题解析:由图中电极材料及电解质溶液可判断B池为电解池,A池、C池符合原电池条件,但由于Ag-Zn活动性差别比Ag-Cu活动性差别大,所以Ag-Zn原电池更容易放电,若A池、C池相连则C池为电解池,C池符合电镀条件,因此C池为电镀池。A池①极为原电池负极,电极反应Zn-2e-===Zn2+,B池③极为阳极,电极反应为2Cl--2e-===Cl2↑,C池⑤极发生:2Ag-2e-===2Ag+,由得失电子守恒可求出①、⑥电极上质量的变化;C池是电镀池,电镀过程中电解质溶液的浓度不变。
本题难度:一般
|
|