微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 25℃时,在某物质的溶液中,由水电离出的c(H+)=1×10-a mol/L,下列说法正确的是?( )
A.a<7时,溶液的pH一定为a
B.a>7时,溶液的pH一定为14-a
C.a>7时,溶液的pH可能为a也可能为14-a
D.a<7时,水的电离受到抑制
参考答案:C
本题解析:
试题分析:a<7时,说明该溶液中水的电离是被促进的,而a>7时,该溶液中水的电离被抑制。酸或碱都是可以抑制水的电离,而盐类的水解可以促进水的电离,所以由水电离出的c(H+)=1×10-a mol/L的溶液的酸碱性无法确定,所以A、B、D都错误,C正确。答案选C。
点评:水是一种弱电解质,存在电离平衡,所以根据水的电离平衡方程式H2O
本题难度:一般
2、计算题 (5分)在100mL 2mol/L的Ba(OH)2溶液中滴加100mL NaHSO4溶液,测得溶液的pH为1,求产生的沉淀的质量?
参考答案:反应后溶液的pH=1
说明硫酸氢钠是过量的
因为
本题解析:考查pH和根据方程式进行的有关计算。
本题难度:一般
3、选择题 室温时,把10 mL pH=10的强碱溶液小心地加入到10 mL pH=4的某酸溶液中,在完全反应后的溶液中滴入紫色的石蕊试液时,溶液显红色,则此酸为???????????? (??? )
A.一元强酸
B.二元强酸
C.任何强酸
D.弱酸
参考答案:D
本题解析:如果酸为强酸,则两溶液中的H+与OH―恰好中和,溶液呈中性,而实际上混合溶液呈酸性,则只能说明弱酸溶液中存在电离平衡,不断电离出H+,故答案为D,但酸的元数无法确定
本题难度:简单
4、选择题 将 pH值相同的盐酸和醋酸稀溶液,分别用蒸馏水稀释至原体积的m倍和 n倍后,两溶液的 pH值仍然相同,则m和n的关系是
A.m<n
B.m>n
C.m=n
D.不能确定
参考答案:A
本题解析:m与n谁大谁小呢?假设m=n,即稀释相同的倍数(如100倍),则盐酸的pH值上升2个单位。假如醋酸的电离平衡不动,则pH值也应上升2个单位。但实际上醋酸因稀释电离度增大,故H+数目有所增加,故其pH值的增大应不足2个单位(比盐酸的pH值小),因此,欲使其pH值与盐酸相同,还必须再加一些水,即m<n。
本题难度:一般
5、选择题 下列化学式表示的粒子对H2O的电离平衡不产生影响的是
A.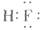
B.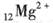
C.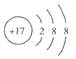
D.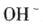
参考答案:C
本题解析:水是一种弱电解质,存在电离平衡,方程式为H2O H++OH-。所以酸或碱能抑制水的电离,而发生水解的某些盐促进水的电离,A、D抑制水的电离,镁离子水解促进水的电离,氯离子既不能促进也不能抑制水的电离,答案选C。
H++OH-。所以酸或碱能抑制水的电离,而发生水解的某些盐促进水的电离,A、D抑制水的电离,镁离子水解促进水的电离,氯离子既不能促进也不能抑制水的电离,答案选C。
本题难度:一般