微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 正确掌握化学用语是学好化学的基础,下列有关化学用语正确的是
A.HCO3-的水解方程式:HCO3-+H2O?H3O++CO32-
B.乙烯的燃烧热是bkJ/mol ,表示燃烧热的热化学方程式为C2H4(g)+3O2(g)=2CO2(g)+2H2O(g)△H=-bkJ/mol
C.以铜为电极电解氯化铜溶液::Cu2++2Cl-== Cu +Cl2↑。
D.在酸性碘化亚铁溶液中通入少量氧气:4I-+ O2 + 4H+ = 2I2 + 2H2O
参考答案:D
本题解析:
试题分析:A、碳酸氢根离子水解生成碳酸和氢氧根离子,错误;B、乙烯燃烧热是指1mol的乙烯完全燃烧生成二氧化碳和液态水时放出的热量,不是水蒸气,错误;C、铜作电极时,电解池的阳极则是Cu失去电子,不是氯离子,所以不会产生氯气,错误;D、氧气与酸性的KI发生氧化还原反应生成碘单质和水,符合离子方程式的书写,正确,答案选D。
考点:考查离子方程式书写正误的判断
本题难度:一般
2、填空题 (9分)某强酸性溶液X中可能含有H+、A13+、NH4+、Fe2+、CO32-、SO42-、C1-、NO3- 中的若干种。某研究性小组为了探究其成分,进行了如下实验:
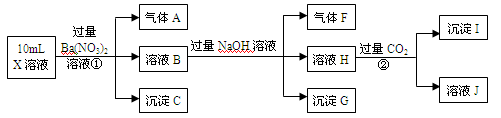
请回答下列问题:
(1)沉淀C的化学式为 ,气体A的化学式为 。
(2)写出向溶液H中通入过量CO2气体生成沉淀I的离子方程式: 。
(3)通常可以利用KClO在KOH溶液中氧化沉淀G来制备一种新型、高效、多功能水处理剂K2MO4。(M为G中的一种元素,K2MO4易溶于水)请写出制备过程中的离子方程式(M用具体的元素符号表示) 。
(4)无法确定的离子是 ,请设计实验验证该离子是否存在的方法 。
参考答案:(1)BaSO4 NO (各1分)(2
本题解析:
试题分析:溶液显强酸性,则一定不存在碳酸根离子,存在氢离子。混合液中加入过量硝酸钡溶液,产生气体A、溶液B和沉淀C,这说明溶液中一定有还原性离子在酸性溶液中被硝酸根氧化,因此一定含有亚铁离子。在强酸性溶液中硝酸根能氧化亚铁离子,则硝酸根一定不存在,气体A是NO,C是硫酸钡,所以含有硫酸根离子。B中加入过量的氢氧化钠溶液又产生气体F、溶液H和沉淀G,则F一定是氨气,即含有铵根。G中一定存在氢氧化铁。H中加入过量的CO2沉淀溶液J和沉淀I,则I应该是氢氧化铝,即H中含有偏铝酸钠,因此原溶液中含有铝离子。
(1)根据以上分析可知沉淀C的化学式为BaSO4,气体A的化学式为NO。
(2)向溶液H中通入过量CO2气体生成沉淀I的离子方程式为[Al(OH)4]-+CO2==Al(OH)3↓+HCO3-。
(3)次氯酸钾氧化氢氧化铁生成高铁酸钾的离子方程式为3ClO-+2Fe(OH)3+4OH-=2FeO42-+3Cl-+5H2O。
(4)根据以上分析可知无法确定的离子是C1-。由于溶液中的硫酸根离子能干扰氯离子的检验,则验证该离子是否存在的方法为取少量的B溶液于试管中,(滴加稀硝酸酸化),滴加AgNO3溶液,若有白色沉淀生成,证明含有C1-;若无白色沉淀生成,证明不含C1-。
考点:考查离子共存与检验的应该分析判断
本题难度:困难
3、选择题 下列各反应,能用同一离子方程式表示的是 ( )
A.氢氧化钠与盐酸;氢氧化铜与盐酸
B.氯化钡溶液与硫酸铜溶液;氢氧化钡溶液与硫酸铜溶液
C.Na2CO3溶液与硝酸溶液; CaCO3与硝酸溶液
D.石灰石与硝酸反应;石灰石与盐酸
参考答案:D
本题解析:
试题分析:A.氢氧化铜为弱碱,离子反应中应保留化学式,则不能用同一离子方程式表示,故A不选;B.氯化钡与硫酸铜反应本质是Ba2++SO42-=BaSO4但氢氧化钡溶液与硫酸铜溶液反应不但生成硫酸钡还能生成氢氧化铜,故不能用同一离子方程式表示,故B不选;C.碳酸钠为溶于水的盐,而碳酸钙是难溶于水的盐,则不能用同一离子方程式表示,故C不选;D.反应实质均为碳酸钙与氢离子反应,盐酸和硝酸都是强酸,则能用同一离子方程式表示,故D选;
考点:离子方程式的书写
本题难度:一般
4、选择题 下列离子方程式正确的是
A.用铂电极电 解氯化镁溶液:2Cl-+ 2H2O
解氯化镁溶液:2Cl-+ 2H2O 2OH-+ Cl2↑+H2↑
2OH-+ Cl2↑+H2↑
B.Fe(OH) 3溶于氢碘酸:Fe(OH)3+3H+===Fe3++3H2O
3溶于氢碘酸:Fe(OH)3+3H+===Fe3++3H2O
C.稀硝酸和过量的铁屑反应:3Fe+8H++2NO3―===3Fe3++2NO↑+4H2O
D.含等物质的量的NaHCO3和Ba(OH)2溶液混合:
HCO3―+OH-+Ba2+ ===BaCO3↓+H2O
参考答案:D
本题解析:略
本题难度:一般
5、选择题 下列表示对应化学反应的离子方程式正确的是
A.将过量SO2通入冷氨水中:SO2+NH3・H2O HSO3-+NH4+
HSO3-+NH4+
B.向NH4HCO3溶液中加过量的NaOH溶液并加热:NH4++OH- NH3↑+H2O
NH3↑+H2O
C.用KIO3氧化酸性溶液中的KI:5I-+IO3-+3H2O 3I2+6OH-
3I2+6OH-
D.用稀硝酸洗涤试管内壁的银镜:Ag+2H++NO3- Ag++NO↑+H2O
Ag++NO↑+H2O
参考答案:A
本题解析:
试题分析:A.将过量SO2通入冷氨水中:SO2+NH3・H2O HSO3-+NH4+,故A正确。B.漏掉了HCO3-与OH-的反应,故B错误。C.酸性溶液中不会生成OH-,故C错误。D.不符合电子守恒,故D错误。
HSO3-+NH4+,故A正确。B.漏掉了HCO3-与OH-的反应,故B错误。C.酸性溶液中不会生成OH-,故C错误。D.不符合电子守恒,故D错误。
考点:了解离子反应的概念、离子反应方程式的书写。
点评:离子方程式正误判断要在掌握基本方法的基础上,针对反应中物质的性质、反应的条件、物质的用量、反应的环境等因素具体分析,正确判断。特别是氧化还原反应的离子方程式书写一定符合“三守恒”:原子守恒,电荷守恒和电子守恒。
本题难度:一般