微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 下列各离子组,因发生氧化还原反应而不大量共存的是
A.K+ Na+ HSO3- NO3-
B.Mg2+ Al3+ SO42- OH-
C.K+ Fe2+ Cl- S2-
D.K+ Ba2+ NO3- SO32-
参考答案:A
本题解析:BCD是因为复分解反应而不能大量共存,A中HSO3-会发生部分电离而使溶液显酸性,又有NO3-会氧化HSO3-。故选A。
本题难度:一般
2、选择题 在溶液中加入足量Na2O2后仍能大量共存的离子组是( )。
A.NH4+、Ba2+、Cl-、NO3-
B.K+、AlO2-、Cl-、SO42-
C.Ca2+、Mg2+、NO3-、HCO3-
D.Na+、Cl-、CO32-、SO32-
参考答案:B
本题解析:在溶液中加入Na2O2固体,Na2O2首先与水反应生成NaOH和O2,A中,NH4+和OH-因发生反应生成NH3・H2O而不大量共存;C中Ca2+、
Mg2+、HCO3-和OH-都不能大量共存;D中SO32-具有还原性,和Na2O2、O2都会发生氧化还原反应,因此答案为B。
本题难度:一般
3、选择题 下列能大量共存于溶液中的一组离子是[???? ]
A.Fe3+、K+、SCN-、SO42-??
B.Fe3+、Fe2+、H+、S2-
C.Mg2+、Fe2+、OH-、NO3-??
D.Na+、Fe3+、NO3-、Cl-
参考答案:D
本题解析:
本题难度:一般
4、计算题 (1)已知25℃时有关弱酸的电离平衡常数:
弱酸化学式
| HSCN
| CH3COOH
| HCN
| H2CO3
|
电离平衡常数
| 1.3×10―1
| 1.8×10―5
| 4.9×10―10
| K1=4.3×10―7? K2=5.6×10―11
?
①等物质的量浓度的a.CH3COONa、b.NaCN、c.Na2CO3、d.NaHCO3溶液的pH由大到小的顺序为
???????????????????????(填序号)。
②25℃时,将20 mL 0.1 mol・L―1 CH3COOH溶液和20 mL 0.1 mol・L―1HSCN溶液分别与20 mL 0.1 mol・L―1NaHCO3溶液混合,实验测得产生的气体体积(V)随时间(t)的变化如图所示:反应初始阶段两种溶液产生CO2气体的速率存在明显差异的原因是 ?????????????????????????????????????。反应结束后所得两溶液中,c(CH3COO―)????c(SCN―)(填“>”、“<”或“=”)
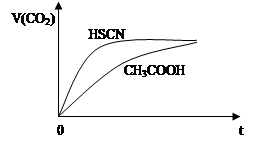
③若保持温度不变,在醋酸溶液中加入少量盐酸,下列量会变小的是______(填序号)。
a. c(CH3COO-)?? b. c(H+)?? c. Kw????????????????d. 醋酸电离平衡常数?
(2)下图为某温度下,PbS(s)、ZnS(s)、FeS(s)分别在溶液中达到沉淀溶解平衡后,溶液的S2―浓度、金属阳离子浓度变化情况。如果向三种沉淀中加盐酸,最先溶解的是???????????(填化学式)。向新生成的ZnS浊液中滴入足量含相同浓度的Pb2+、Fe2+的溶液,振荡后,ZnS沉淀会转化为??????????????(填化学式)沉淀。
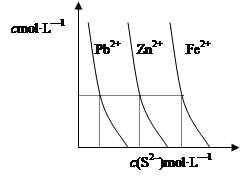
(3)甲烷燃料电池可以提升能量利用率。下图是利用甲烷燃料电池电解50 mL 2 mol・L―1的氯化铜溶液的装置示意图:
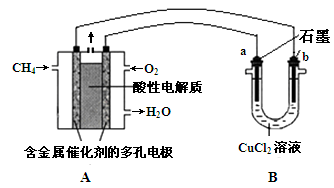
请回答:
① 甲烷燃料电池的负极反应式是??????????????????????????????????????????。
② 当线路中有0.1 mol电子通过时,???????极增重________g
参考答案:(13分)(1)① c b d a?(2分)
②同浓度
本题解析:
试题分析:(1)①电离平衡常数越小,酸越弱,因此根据电离平衡常数可知,酸性强弱顺序是HSCN>CH3COOH>H2CO3>HCN>HCO3-。酸越弱,相应的钠盐越容易水解,溶液的pH越大,则等物质的量浓度的a.CH3COONa、b.NaCN、c.Na2CO3、d.NaHCO3溶液的pH由大到小的顺序为c>b>d>a。
②根据电离常数可知,同浓度的HSCN比CH3COOH酸性强,所以与NaHCO3溶液反应快;反应结束后得到的是醋酸钠后NaSCN溶液。由于酸性是HSCN比CH3COOH酸性强,所
本题难度:困难
5、填空题 (15分)现有A、B、C、D、E、F六种常见化合物 ,均为强电解质,它们的阳离子有Al3+、NH+4、Na+、Ag+、H+五种,阴离子有Cl-、HCO-3、OH-、NO-3、SO2-4五种,现将它们分别配成0.lmol/L。的溶液,进行如下实验: ,均为强电解质,它们的阳离子有Al3+、NH+4、Na+、Ag+、H+五种,阴离子有Cl-、HCO-3、OH-、NO-3、SO2-4五种,现将它们分别配成0.lmol/L。的溶液,进行如下实验:
①测得A溶液呈碱性,E溶液的pH为1,C溶液的酸性强于E溶液。
②向B溶液中滴入D溶液,出现白色沉淀和无色无味气体,该白色沉淀既能溶于A溶液,又能溶于C溶液;过滤,向滤液中加入A溶液,加热,有刺激性气味气体产生。
③向B溶液中滴加F溶液,产生白色沉淀,加入过量E溶液,沉淀不溶解。
④向E溶液中滴加F溶液,无明显变化。
根据上述实验现象,回答下列问题:
(1)写出下列四种化合物的化学式:
A 、B 、D 、F 。
(2)C溶液是 ,判断依据是____
(3)B、D反应的离子方程式是____ ;
参考答案:(15分)
 本题解析:略 本题解析:略
本题难度:一般
|