微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 下列仪器:①烧杯②坩埚③蒸发皿④试管⑤烧瓶,用酒精灯加热时,需垫石棉网的是
A.②④
B.①⑤
C.③④
D.①③
参考答案:B
本题解析:考查常见仪器的使用。烧杯和烧瓶在加热时,需要垫石棉网,其余是不需要的,所以正确的答案选B。
本题难度:一般
2、填空题 工业上以锂辉石(Li2O・Al2O3・4SiO2,含少量Ca、Mg元素)为原料生产碳酸锂。其部分工艺流程如下:

已知:①Li2O・Al2O3・4SiO2 H2SO4(浓)
H2SO4(浓) Li2SO4
Li2SO4 Al2O3・4SiO2・H2O↓
Al2O3・4SiO2・H2O↓
②某些物质的溶解度(S)如下表所示:
T/℃
| 20
| 40
| 60
| 80
|
 (Li2CO3)/g (Li2CO3)/g
| 1.33
| 1.17
| 1.01
| 0.85
|
 (Li2SO4)/g (Li2SO4)/g
| 34.2
| 32.8
| 31.9
| 30.7
?
③从滤渣1中提取出Si的部分流程如下图所示:

根据以上信息,请回答下列问题:
(1)括号内应提供的相应条件和物质 ???????? 、 ????? 。
(2)方框中所得物质的化学式 ?????? 。
(3)使用浓硫酸并加热到250℃~300℃的目的是 ?????????????? 。
(4)②处加Na2CO3溶液所发生反应的离子方程式 ?????????????????? ?、 ?????????????????????????????????????????????。
(5)滤渣2的主要成分有 ??????????????????????? 。
(6)如何检验Li2CO3是否洗涤干净? ????????????????????????? 。
参考答案:(1)加热或高温(1分)??????C和高温?? (2分)?
本题解析:
试题分析:H4SiO4加热生成SiO2,SiO2与C在高温条件下反应生成单质Si和CO,所以(1)括号内相应条件和物质分别为加热、C和高温;(2)方框中物质为H4SiO4加热分解的产物:SiO2。
(3)使用浓硫酸并加热到250℃~300℃的目的是减少杂质的溶解、提高Li2SO4的浸出率、加快浸出速率。
(4)加入H2SO4后生成CaSO4,CaSO4微溶,含Ca2+和CaSO4固体,所以加入Na2CO3反应的离子方程式为:Ca2+?+CO32- =CaCO3↓、CaSO4+CO32-
本题难度:一般
3、选择题 下列实验操作正确的是:??????????????????????(???? )
A.蒸发结晶时,边加热边用玻璃棒搅拌直至溶液蒸干为止
B.配制100mL浓度约2mol・L-1 的NaOH溶液,将8gNaOH放入烧杯中加入92g水溶解
C.不慎将酸溅到眼中,应立即用水冲洗,边洗边揉眼睛
D.滴瓶上的胶头滴管用完后要洗净后再放回原瓶
参考答案:B
本题解析:略
本题难度:一般
4、选择题 下列操作或仪器的选用正确的是 [???? ]
A.滴定FeSO4溶液?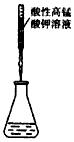
B.制取O2
C.制备Fe(OH)2 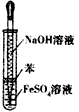
D.稀释浓硫酸 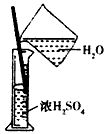
参考答案:C
本题解析:
本题难度:一般
5、选择题 下列说法正确的是
A.配制FeCl3溶液,可将一定量FeCl3固体溶于适量盐酸中并加入少量铁粉
B.制备Fe(OH)3胶体,可向沸水中滴加FeCl3饱和溶液并长时间煮沸
C.配制0.1 mol・L-1 NaOH溶液100 mL,将4.0 g NaOH固体放入100 mL容量瓶中溶解
D.向饱和Ca(OH)2溶液中加入少量无水CaO固体,恢复原温度,溶液中Ca(OH)2的物质的量浓度不变
参考答案:D
本题解析:
试题分析:配制FeCl3溶液,可将一定量FeCl3固体溶于适量盐酸中,不能加入少量铁粉,因为Fe+2Fe3+=3Fe2+,故A错误;制备氢氧化铁胶体时,当溶液变为红褐色时应立即停止加热,如长时间煮沸会导致?胶体聚沉,故B错误;配制0.1 mol・L-1 NaOH溶液100 mL,将4.0 g NaOH固体不能放入100 mL容量瓶中溶解,应放入烧杯中溶解,,故C错误;向饱和Ca(OH)2溶液中加入少量无水CaO固体,恢复原温度,还是饱和溶液,所以溶液中Ca(OH)2的物质的量浓度不变,故D正确。故
本题难度:一般
|