��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1��ѡ���� ����ͬ�¶Ⱥ�ѹǿ��,���������ܶ���С����
A��CO2
B��H2
C��O2
D��Cl2
�ο��𰸣�B
���������
�����������ͬ�¶Ⱥ�ѹǿ��,�����ܶ�֮�Ⱦ�����Է�������֮�ȣ���������Է���������С�ģ�ѡB��
���㣺���鰢��٤�����ɼ����ۡ�
�����Ѷȣ�һ��
2��ѡ���� ��NAΪ�����ӵ���������ֵ������˵����ȷ���ǣ����ԭ��������H 1��N 14��
A��1.8g��NH4+�������NA������
B����״���£�22.4Lˮ�к���NA��H2O����
C�����³�ѹ�£�33.6 L Cl2�к���1.5NA��C12����
D��1 mol��L-1 Na2SO4��Һ����2NA��Na+
�ο��𰸣�A
���������A��ȷ��1.8g��NH4+�������ʵ���Ϊ0.1mol����NH4+����Ϊ10�������ӣ�����1.8g��NH4+�����к���NA�����ӣ�
B������״����ˮΪ��ˮ�����������壻
C���������ڱ�״���µ����
D����û����Һ���������������ʵ�����Ҳ�����ó���������
�����Ѷȣ�һ��
3������� ��6�֣������ʵ�����CO��CO2������Oԭ�Ӹ���֮��????????�����ߵ�����֮��????????����ͬ��ͬѹ�µ����֮��????????��
�ο��𰸣���6�֣�1:2��7:11��1:1
���������
�������������CO2��CO�Ļ�ѧʽ��֪�������ʵ�����ȵ������£�CO��CO2������ԭ�ӵĸ���֮����1�U2�����ߵ�����֮����28�U44��7:11�����ݰ����ӵ����ɿ�֪������ͬ�����£����ߵ����֮����1�U1��
�������ڽ������ʵ������йؼ���ʱ���ؼ�������Ӧ�ü�����ϵʽ ��n��m/M��
��n��m/M��
�����Ѷȣ�һ��
4�������� ���к�H2SO4��K2SO4��Ϊ0.5mol��L-1 �Ļ��Һ300mL��Ϊ���Ƴɺ�H2SO4��K2SO4���ʵ���Ũ�ȷֱ�Ϊ2mol��L-1��0. 2mol��L-1�Ļ��Һ����������ʵ����ʵ���Ũ��Ϊ18.4mol��L-1��Ũ������ٺ�����Ȼ���ټ�ˮϡ�ͣ�
�ο��𰸣�73. 4mL��
���������
�����Ѷȣ�һ��
5�������� ij������Ļ�ѧʽ�ɱ�ʾΪ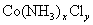 ��x��yΪ����������Ϊ��ȷ��x��y��ֵ��ȡ����������Ϊ0.2140g�ĸû����������������ʵ�顣��һ����������ˮ����������ڵ���������
��x��yΪ����������Ϊ��ȷ��x��y��ֵ��ȡ����������Ϊ0.2140g�ĸû����������������ʵ�顣��һ����������ˮ����������ڵ���������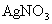 ��Һ�ζ�������
��Һ�ζ�������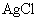 ��������������24.0mL 0.100mol/L��
��������������24.0mL 0.100mol/L��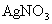 ��Һ������һ�������м������
��Һ������һ�������м������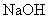 ��Һ�����ȣ����������������ݳ���
��Һ�����ȣ����������������ݳ���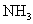 ������
������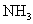 ������24.0mL 0.200mol/L
������24.0mL 0.200mol/L 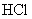 ��Һ����ͨ������ȷ���û�����Ļ�ѧʽ������������õ������ԭ��������HΪ1.00��NΪ14.0��ClΪ35.5��CoΪ58.9��
��Һ����ͨ������ȷ���û�����Ļ�ѧʽ������������õ������ԭ��������HΪ1.00��NΪ14.0��ClΪ35.5��CoΪ58.9��
����
�ο��𰸣����n��ʾ���ʵ�����m��ʾ����
��������������ж��ֽⷨ��ѵ��ѧ���ķ�ɢ˼ά��
����������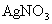 �����ʵ����ɵû�������
�����ʵ����ɵû�������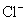 �����ʵ�����������
�����ʵ����������� �����Ѷȣ���
�����Ѷȣ���