��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1������� ��1����ⱥ��ʳ��ˮ�����Ƶ��ռ�������������÷�Ӧ�Ļ�ѧ����ʽΪ��______��
��2���������������뵼����Ϲ���������£�

��3����ʯӢɰ����Ҫ�ɷ���______�����Ʊ��ֹ�ʱ����̿��������______��
�ڴֹ���������Ӧ��õ���Һ̬���Ȼ����г�����һЩ���ʣ�������з����ᴿ�����ᴿ����Ϊ______��
�������Ȼ���õ��ߴ���Ļ�ѧ����ʽ�ǣ�______��
�ο��𰸣���1�����Ե缫��ⱥ��ʳ��ˮ�����������������������ƣ���Ӧ��
���������
�����Ѷȣ�һ��
2��ѡ���� ��ͼ��װ�ý���ʵ�飬��ͼ���к�����x��ʾͨ���缫�ĵ��ӵ����ʵ���������������ȷ���ǣ�???��

A��F��ʾ��Ӧ����Cu�����ʵ���
B��E��ʾ��Ӧʵ������H2O�����ʵ���
C��E��ʾ��Ӧ����O2�����ʵ���
D��F��ʾ��Ӧ����H2SO4�����ʵ���
�ο��𰸣�B
���������
������������Ե缫�������ͭ��Һ����������ͭ��������
���ᣬ��Ӧ�Ļ�ѧ����ʽ��2H2O��2CuSO4=2H2SO4��2Cu��O2����
��������1mol����ת��4mol���ӣ���ת��4mol��������2molͭ������F��ʾ��Ӧ�������������ʵ�����E��ʾ��Ӧ����Cu�����ʵ�����������������ʵ���������ˮ�����ʵ�������������ͭ�����ʵ�������ѡB��
�����������Ǹ߿��еij������ͣ������е��Ѷȵ����⡣�����ۺ���ǿ�����ض�ѧ������֪ʶ�Ĺ��̺�ѵ��������������ѧ�������������������ѧ���������
�����Ѷȣ���
3������� ����13�֣��ȼҵ��������Ļ�ѧ��ҵ֮һ������Ҫԭ�����ڵ�ⱥ��ʳ��ˮ��2NaCl��2H2O 2NaOH��H2����Cl2�������IJ�Ʒ�ռ�������Լ�����Ӧ�ù㷺����ش��������⣺
2NaOH��H2����Cl2�������IJ�Ʒ�ռ�������Լ�����Ӧ�ù㷺����ش��������⣺
��1�����ǰ�����������SO42-�����ϸߣ��������ӱ��Լ���ȥSO42-���ñ��Լ�������______________(����ĸ����)��
A��Ba(OH)2���� B��Ba(NO3)2���� C��BaCl2
��2�������ࡱ�ǵ��ʳ��ˮ�������γɵĹ�ҵ�����ϡ���ij����������������£�
�ɷ�
| NaCl
| Mg(OH)2
| CaCO3
| BaSO4
| ����������
|
��������(��)
| 15��20
| 15��20
| 5��10
| 30��40
| 10��15
������������MgSO4��7H2O����Ĺ�����������ͼ��ʾ��
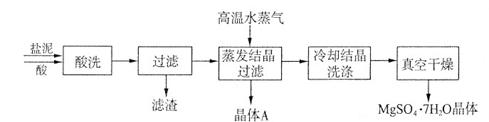
�ش��������⣺
����ϴ�����м��������������pHΪ5���ң���Ӧ�¶���50�����ҡ���������ʹ֮��ַ�Ӧ����ʹMg(OH)2����ܽⲢת��ΪMgSO4��CaCO3�ڴ˹�����ת��ΪCaSO4������ʹ�ת�����Է�����ԭ��_________��
�ڹ���������������Ҫ�ɷ�Ϊ____________________________��
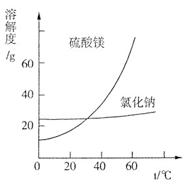
�۸�����ͼ�����������ᾧ�������þ���A��Ҫ�ɷ�Ϊ____________________��
����ո���MgSO4��7H2O�����ԭ����______________________��
��3����֪NaCl��60 ����ܽ��Ϊ37.1 g���ֵ��60 �澫�Ʊ���ʳ��ˮ1371 g����������������Һ�ܶ�Ϊ1.37 g��cm-3�����к���20 g NaCl�������NaOH�����ʵ���Ũ��Ϊ________________mol/L��
�ο��𰸣���1��A��C
��2������������̼��Ʒ�Ӧ����������в�
���������
�����������1�����ǰ�����������SO42-�����ϸߣ��������ӱ��Լ���ȥSO42-���ڳ�ȥ���ʵ�ʱ������Ҫ�����µ��������ӣ����Ըñ��Լ�������A��Ba(OH)2��C��BaCl2��(2)����ϴ�����м��������������pHΪ5���ң���Ӧ�¶���50�����ҡ���������ʹ֮��ַ�Ӧ����ʹMg(OH)2����ܽⲢת��ΪMgSO4��CaCO3�ڴ˹�����ת��ΪCaSO4����ת�����Է�����ԭ������������̼��Ʒ�Ӧ����������в�����CO2�����ݳ���̼���ת��Ϊ����ƣ��ڹ���������������Ҫ�ɷ�ΪBaSO4��CaSO4�Ȳ�����������ʣ��۸������ʵ��ܽ�����¶ȵĹ�ϵ��֪��NaCl���ܽ�����¶ȵ�Ӱ��仯��С����MgSO���ܽ�����¶ȵ�Ӱ��仯�ϴ����Բ��������ܼ���MgSO4�ͻ��Ϊ������Һ�����������ͻ��������壬�õ�����Һ��Ҫ�ɷ���NaCl.�����������ܼ��õ��ľ�����Ҫ��NaCl������ո���MgSO4��7H2O�����ԭ���Ǽ�Сѹǿ������ˮ�ķе㣬��������¶ȹ��߶�ʧȥ�ᾧˮ��3������NaCl��60 ����ܽ��Ϊ37.1 g�����Ե��60 �澫�Ʊ���ʳ��ˮ1371 g�������к���NaCl371g,H2O��1000g����������������Һ�ܶ�Ϊ1.37 g��cm-3�����к���20 g NaCl�������NaCl��������371g��20 g=351g,���ݵ��ķ���ʽ�ǣ�2NaCl��2H2O 2NaOH��H2����Cl2������֪ÿ��Ӧ����117gNaCl�ͻ����2mol��NaOH,��������80g,�ų�������������1mol,���ڷ�Ӧ��NaCl��351g���������NaOH�����ʵ����ǣ�351g��117g����2mol=6mol���ų����������������ʵ�������3mol,���Է�Ӧ����Һ��������1371 g��3mol��2g/mol��3mol��71g/mol=1152g��������Һ������ǣ�1152g��1.37 g��cm-3=840.9ml=0.8409L,���Ե���NaOH�����ʵ���Ũ��Ϊc=n��V=6mol��="0.8409L" =7.14mol/L�� 2NaOH��H2����Cl2������֪ÿ��Ӧ����117gNaCl�ͻ����2mol��NaOH,��������80g,�ų�������������1mol,���ڷ�Ӧ��NaCl��351g���������NaOH�����ʵ����ǣ�351g��117g����2mol=6mol���ų����������������ʵ�������3mol,���Է�Ӧ����Һ��������1371 g��3mol��2g/mol��3mol��71g/mol=1152g��������Һ������ǣ�1152g��1.37 g��cm-3=840.9ml=0.8409L,���Ե���NaOH�����ʵ���Ũ��Ϊc=n��V=6mol��="0.8409L" =7.14mol/L��
���㣺������εij������ᴿ�������ķ��롢ʳ��ˮ�ĵ��һ��������ʵ���Ũ�ȵļ����֪ʶ��
�����Ѷȣ�һ��
4��ѡ���� ������������Ni2O3��������������ܵ�أ����ⷨ�Ʊ��������£���NaOH��NiCl2��ҺpH��7��5���������������ƺ���е�⡣�������в�����Cl2������������������ClO-���Ѷ���������Ϊ������������˵����ȷ����[???? ]
A������������������
B��������������������Һ��pH����
C��������Ӧ����ʽ�ǣ�2Cl--2e-===Cl2
D��������ʹ1mol������ת��Ϊ�����������Cl2�����·��ͨ����1mol����
�ο��𰸣�CD
���������
�����Ѷȣ�һ��
5��ѡ���� �ö��Ե缫���һ����������ͭ��Һ��ʵ��װ����ͼ1��ʾ���������е�ʵ��������ͼ2��ʾ���������ʾ��������ת�Ƶ��ӵ����ʵ������������ʾ�������в����������������������������˵������ȷ����
 
A���������У�b�缫�������к�ɫ����������Ȼ��������ݲ���
B���ӿ�ʼ��Q��ʱ�ռ����Ļ�������ƽ����Է�������Ϊ17
C������OP �α�ʾH2��O2������������仯������PQ�α�ʾO2������仯
D��a�缫�Ϸ�����Ӧ�ķ���ʽΪ��2H+ + 2e- = H2����4OH-�C4 e-=2H2O+ O2��
�ο��𰸣�B
���������
���������A.���ݵ��װ��ʾ��ͼ��֪b��������a�������������ڵ������У�a�缫�������к�ɫ����������Ȼ��������ݲ���.����B���ӿ�ʼ��P�㣬b�缫������Ӧ��4OH-��4e-=2H2O+O2��; V(O2)=1.12L,������������Ӧ��Cu2++2e-=Cu,�������ʵ���ǵ��ˮ��2H2O 2H2�� + 2H2�� +
�����Ѷȣ�һ��
|