微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 氮氧化铝(AlON)是一种透明高硬度防弹材料,可以由反应Al2O3+C+N2=2AlON+CO(高温)合成,下列有关说法正确的是
A.氮氧化铝中氮的化合价是-3
B.反应中氮气作氧化剂
C.反应中每生成5.7g AlON 同时生成1.12 L CO
D.反应中氧化产物和还原产物的物质的量之比是2:1
参考答案:B
本题解析:
试题分析:A、O元素的化合价为-2,Al的化合价为+3价,所以氮氧化铝中N的化合价是-1价,错误;B、N元素的化合价降低,被还原,作氧化剂,正确;C、5.7gAlON的物质的量是0.1mol,每生成0.1molAlON同时生成0.05molCO,但CO的体积因为未指明条件而不能确定,错误;D、反应中的还原产物是AlON,氧化产物是CO,所以氧化产物与还原产物的物质的量之比是1:2,错误,答案选B。
考点:考查氧化还原反应的分析,元素化合价的判断,氧化剂、还原剂、氧化产物、还原产物的判断
本题难度:一般
2、选择题 科学家发现C60后,近年又合成了许多球形分子(富勒烯),如C50、C70、C120、C540等,它们互称为
A.同种物质
B.同分异构体
C.同素异形体
D.同位素
参考答案:C
本题解析:
试题分析:根据由同一元素形成的不同单质称为同素异形体;同分异构体是分子式相同结构式不同的化合物;结构和性质完全相同的是同一种物质;质子数相同中子数不同原子互称同位素;C50、C70、C120、C540等物质都是由碳元素组成的单质,是同素异形体,故选:C;
本题难度:一般
3、简答题 (1)分别取Wg钠、镁、铝与足量的盐酸反应,在相同条件下产生氢气的体积比是______;
(2)分别取0.1mol钠、镁、铝与足量的盐酸反应,在相同条件下产生氢气的体积比是______;
(3)若产生相同物质的量的氢气,所需钠、镁、铝的质量比为______;
(4)若产生相同体积(同温同压下)的氢气,所需钠、镁、铝三种金属的物质的量之比为______;
(5)若将0.2mol金属钠、铝、铁分别投入到10mL1mol/L的盐酸中,在标准状况下,产生氢气的体积大小顺序是______;
(6)把0.5mol钠投入到m1g水(过量)中得到a溶液,把0.5mol镁投入到m2g盐酸(过量)中得到b溶液,若m1=m2,则a、b质量的大小关系是______.
参考答案:涉及到的化学方程式有①2Na+2HCl=2NaCl+H2↑,
本题解析:
本题难度:简单
4、选择题 物质X(

)和物质Y(
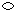
)的反应中,微粒之间的关系如图所示,对该反应的描述,下列反应方程式正确的是( )
A.3X+8Y→X3Y8
B.X+2Y→XY2
C.3X+6Y→X3Y6
D.3X+8Y→3XY2+2Y
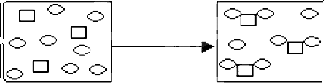
参考答案:根据反应容器中物质X和物质Y的反应微粒之间的关系图,图中的3
本题解析:
本题难度:一般
5、填空题 请解决以下有关氧化还原反应的问题:
(1)在MnO2+4HCl(浓) MnCl2+2H2O+Cl2↑的反应中,用双线桥法标出电子转移的方向和数目:????????????????????????????????????????????????
MnCl2+2H2O+Cl2↑的反应中,用双线桥法标出电子转移的方向和数目:????????????????????????????????????????????????
在上述反应中,作氧化剂的是???????????,作还原剂的是???????????,氧化产物是????????????。
(2)铁钉浸入CuSO4溶液后,表面会附有红色物质;铜丝浸入AgNO3溶液后,表面会附有银白色物质,则在Cu、Fe、Ag中,__ ______原子还原性最强;在Cu2+、Fe2+、Ag+中,__ _______离子氧化性最强。
参考答案:
 本题解析:略
本题解析:略
本题难度:简单