微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 下表是部分短周期元素的原子半径及主要化合价,根据表中信息,判断以下叙述正确的是(??)????
元素代号
| L
| M
| Q
| R
| T
|
原子半径/nm
| 0.160
| 0.134
| 0.089
| 0.102
| 0.074
|
主要化合价
| +2
| +3
| +2
| +6、-2
| -2
A.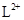 与 与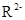 的核外电子数相等 的核外电子数相等
B.L与T形成的化合物具有两性
C.氢化物的稳定性为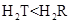
D.单质与浓度相等的稀盐酸反应的速率为Q<L
2、选择题 下列各组元素中,电负性依次减小的是
A.K、Na、Al
B.O、Cl、H
C.As、P、H
D.O、S、Cl
3、选择题 下列比较中,正确的是:??????(??)
A.离子半径:S2―>Cl―>Na+>Mg2+
B.热稳定性:H2S<H2Se<HCl
C.酸性:HF>HCl>HBr>HI
D.氧化性:F2>Cl2> P > S
4、选择题 关于下列图示的说法中正确的是
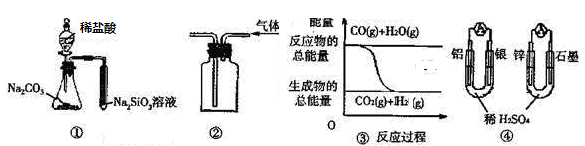
A.用图 ① 所示实验可比较氯、碳、硅三种元素的非金属性强弱
B.用图 ② 所示实验装置排空气法收集CO2气体
 | C.图 ③ 表示反应 CO(g)+H2O(g) CO2(g)+H2(g)是放热反应
D.图 ④ 两个装置中通过导线的电子数相同时,消耗负极材料的物质的量也相同
5、填空题 (12分)根据所学物质结构知识,请你回答下列问题:
(1)人们把电子云轮廓图称为原子轨道,S电子的原子轨道都是??????形的,P电子的原子轨道都是??????????形的。
(2)原子序数为24的元素原子中有????个能层,????个能级,??????个未成对电子。
(3)硅原子核外电子排布式为?????????????????,价电子排布式为???????????
(4)NCl3常温下为黄色粘稠的油状液体,可用作引爆剂和化学试剂。NCl3分子的VSEPR模型是????????????,立体构型是???????????,中心原子采取????????杂化方式。
(5)具有(n-1)d10ns2电子构型的元素位于周期表中???????区和??????族。
|