微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、简答题 (16分)工业上需要利用一批回收的含铜废料制造胆矾(CuSO4・5H2O)。该废料中各种成份含量如下:Cu和CuO约占87%,其它为Mg、Al、Fe、Si及其氧化物,还有少量的难溶物质。工艺流程为:
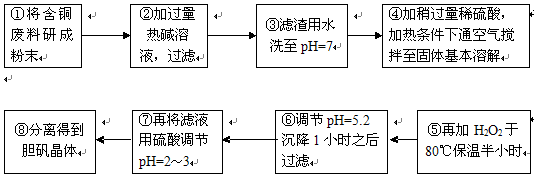
部分金属阳离子以氢氧化物形式完全沉淀时溶液的pH如下表:
沉淀物
| Al(OH)3
| Fe(OH)3
| Cu(OH)2
| Mg(OH)2
| Fe(OH)2
|
pH
| 5.2
| 3.1
| 6.7
| 9.4
| 9.7
回答:
(1)步骤①中为什么要将含铜废料研磨成粉状?
??????????????????????????????????????????????????????????????????。
(2)步骤②中的离子方程式(写出2个即可):
??????????????????????????????、????????????????????????????????????。
步骤⑤中H2O2参加反应的离子方程式:??????????????????????????????????。
(3)步骤⑥中调节溶液pH时适宜的物质是???????????????(填序号);
A.NaOH???? B.氨水??? C.Cu2(OH)2CO3??? D.Cu(OH)2????? E.MgCO3
步骤⑥中滤渣成份的化学式?????????????????????????????。
(4)步骤⑦中用硫酸调节pH=2~3的原因是????????????????????????????????????。
步骤⑧的分离方法是??????????????????????????????????????????????????????。
参考答案:(16分)(1)增大固体反应物的表面积,增大化学反应的速率。
本题解析:(1)将含铜废料研磨成粉状,可以)增大固体反应物的表面积,增大化学反应的速率。
(2)废料中能和氢氧化钠反应的是铝、硅、氧化铝和二氧化硅,所以方程式为2Al+2OH-+2H2O=2AlO2-+3H2↑、Si+2NaOH+H2O=Na2SiO3+2H2↑、Al2O3+2OH-=2AlO2-+H2O、SiO2+2NaOH=Na2SiO3+H2O。双氧水的目的是氧化混合液中的亚铁离子,生成铁离子,以形成氢氧化铁沉淀而除去,所以方程式为2Fe2++H2O2 +2H+=2Fe3++2H2O。
(3)用于
本题难度:一般
2、选择题 “绿色化学”是当今社会提出的一个新概念。在“绿色化学工艺中,理想状态是反应物中原子全部转化为欲制的产物,即原子的利用率为100%。在用丙炔合成甲基丙烯酸甲酯
( )的过程中,欲使原子利用率达到最高,还需要其他的反应物是[???? ] )的过程中,欲使原子利用率达到最高,还需要其他的反应物是[???? ]
A.CO和CH3OH????????
B.CO2和H2O ?????
C.H2和CO2?????
D.CH3OH和H2
参考答案:A
本题解析:
本题难度:简单
3、选择题 下列有关化工生产的说法正确的是
A.将氯气通入澄清石灰水制取漂白粉
B.电解饱和食盐水溶液制取金属钠
C.SO2氧化为SO3时需要使用催化剂,这样可以提高SO2的转化率
D.用98.3%的浓H2SO4吸收SO3,目的是防止形成酸雾,使SO3吸收完全
参考答案:D
本题解析:略
本题难度:简单
4、实验题 (18分)硫酸是化学工业最重要的产品之一,工业制法如下。
(1)生产硫酸最古老的方法是以绿矾为原料,在蒸馏釜中煅烧。反应的化学方程式为:2FeSO4・7H2O Fe2O3+SO2+SO3↑+14H2O。其中三氧化硫与水蒸气同时冷凝便得到硫酸。用如图所示装置模拟用绿矾制硫酸的实验,并检验生成的硫酸和二氧化硫(加热装置已略去)。其中b为干燥的试管 Fe2O3+SO2+SO3↑+14H2O。其中三氧化硫与水蒸气同时冷凝便得到硫酸。用如图所示装置模拟用绿矾制硫酸的实验,并检验生成的硫酸和二氧化硫(加热装置已略去)。其中b为干燥的试管 。 。

①试管b中得到的主要产物是???????????,检验该产物的方法是(结合离子方程式简要说明)??????????????????????????????????????????????????????????????????????。
②为检验反应的另一种生成物,试管c中应加入的试剂是????????????,简述相应的实验现象及结论??????????????????????????????????????????。
③所得硫酸的理论浓度(溶质的质量分数)为????????????????????????????????。
(2)目前,我国采用“接触法”制硫酸,生产设备如图所示:
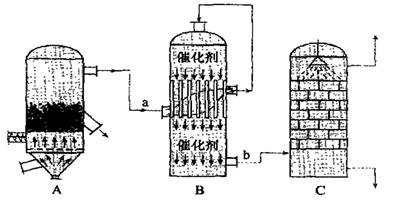
①图中设备A的名称是??????????????????????,a、b两处所含气体的化学式分别为???????????????????????????????、??????????????????????????????。
②有关接触法制硫酸的下列说法中,不正确的是???????????。
A.二氧化硫的接触氧化在合成塔中发生
B.吸收塔得到的 硫酸浓度为98%
C.煅烧含硫48%的黄铁矿时,若FeS2损失了2%,则S损失4%
D. B装置中反应的条件之一为较高温度是为了提高SO2的转化率 B装置中反应的条件之一为较高温度是为了提高SO2的转化率
(3)随着化学工业的发展,“接触法”全面替代了“绿矾热分解法”,请你从综合效益的角度指出“接触法”制硫酸的优势:①生产成本低、②原料易得、③????????????????、④??? ?????????????、⑤???????????????、⑥???????????????(可不填满)。 ?????????????、⑤???????????????、⑥???????????????(可不填满)。
参考答案:(1)① H2SO4(1分);Ba 本题解析:略 本题解析:略
本题难度:一般
5、选择题 绿色化学的目标是[???? ]
A、减少对环境的污染
B、防患于未然,最终杜绝化学污染源
C、设计对人类健康和环境更安全的化合物
D、研究变换基本原料和起始化合物
参考答案:B
本题解析:
本题难度:简单
|