��
.
.
MnC12+C12��+2H2O
�ݴˣ���������������װ����ѡ���Ʊ����ռ�H2��װ��______������ţ����Ʊ����ռ��������C12��װ��______������ţ���
��ѡ���Ʊ������װ�ã�
��3��������Ĥ���۵�ⱥ��ʳ��ˮ������ȡ�����ƣ�ͬʱ�������������Ƶ�������213.0kg������������______m3����״�����������Կ��ܴ��ڵ�������Ӧ��
�ο��𰸣���ⱥ��ʳ��ʱ����������Cl-��OH-�ŵ磬Cl-�ķŵ�����
���������
�����Ѷȣ�һ��
2������� ����ұ���ʹ������漰������ԭ��Ӧ��
��1������������ұ����Ӧ����ʱ���õ�ⷨ���� ��
a��Fe2O3 b��NaCl c��Cu2S d��Al2O3
��2����ͭ��Cu2S���ɷ�����Ӧ2Cu2S+2H2SO4+5O2��4CuSO4+2 H2O���÷�Ӧ�Ļ�ԭ���� ����1mol O2������Ӧʱ����ԭ����ʧ���ӵ����ʵ���Ϊ mol����CuSO4��Һ�м���þ��ʱ���������ɣ��������� ��
��3����ͼΪ��⾫������ʾ��ͼ�� ����a��b����Ϊ�������ʵĴ�������b������������ɫ����ɣ������ɸ�����ĵ缫��ӦʽΪ ��
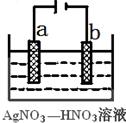
��4��Ϊ������������ĺڰߣ�Ag2S�������������������������ʳ��ˮ�в������Ӵ���Ag2Sת��ΪAg��ʳ��ˮ������Ϊ ��
�ο��𰸣���1��b��d��2�֣�©ѡ��1�֣���ѡ���ѡ��0�֣�
��
���������
�����������1��NaCl��Al2O3ұ����Ҫ�õ�ⷨ��Fe2O3��Cu2S�������Ȼ�ԭ����ѡb��d
��2���ڸ÷�Ӧ�У�CuԪ�ػ��ϼ���+1���ߵ�+2��SԪ�ػ��ϼ���-2���ߵ�+6��Cu2S����ԭ��������1molO2���뷴Ӧת�Ƶĵ���Ϊ4mol������Cu2+ˮ������ԣ�����þ��ʱ��þ��H+��Ӧ������������
��3����⾫��ʱ�������������������������a����b�缫��������������ԭ��Ӧ�������˺���ɫ������NO���������������ɵ�NO2���缫��Ӧ��NO3-+3e-��4H+��NO��+2H2O����NO3-+e-��2H+��NO2��+H2O
��4�����������Һ���γ�ԭ��ء�
���㣺����������ԭ��Ӧ���绯ѧ�Ȼ���֪ʶ��
�����Ѷȣ�����
3�������� ��9�֣�ʵ����ͨ����MnO2��Ũ���Ṳ����ȡCl2����Ӧ�Ļ�ѧ����ʽΪ
MnO2 + 4HCl��Ũ�� MnCl2 + Cl2��+ 2H2O��
MnCl2 + Cl2��+ 2H2O��
��1���÷�Ӧ���������� ������������ ���õ����ŷ���ʾ������Ӧ����ת�Ʒ������Ŀ��
��2�����㵱��73.0��HCl��ȫ�μӷ�ʱ������MnO2�����ʵ���Ϊ���٣����ɵ������ڱ�״���µ������������
�ο��𰸣�
��1��MnO2�� Cl2 &#
���������
�����������1���ɷ���ʽ֪��MnԪ�صĻ��ϼ۽��ͣ���MnO2Ϊ��������ClԪ�ػ��ϼ����ߣ����Ȼ���Ϊ��ԭ��������Ϊ�������MnԪ�صĻ��ϼ���+4�۽���Ϊ+2�ۣ��÷�Ӧ��ת��2e-��ת�Ƶ���Ϊ ��
��
��2������73.0��HCl��ȫ��Ӧʱ��HCl�����ʵ���Ϊ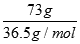 =2mol���ɷ���ʽ��֪����MnO2�����ʵ���Ϊ0.5mol���������������ʵ���Ϊ0.5mol����״���µ����0.5mol��22.4L/mol=11.2L��
=2mol���ɷ���ʽ��֪����MnO2�����ʵ���Ϊ0.5mol���������������ʵ���Ϊ0.5mol����״���µ����0.5mol��22.4L/mol=11.2L��
���㣺������ԭ��Ӧ
�����Ѷȣ�һ��
4��ѡ���� 24 mLŨ��Ϊ0.05 mol��L��1��Na2SO3��Һǡ����20 mLŨ��Ϊ0.02 mol��L��1��K2Cr2O7��Һ��ȫ��Ӧ����֪Na2SO3�ɱ�K2Cr2O7����ΪNa2SO4����Ԫ��Cr�ڻ�ԭ�����еĻ��ϼ�Ϊ (����)��
A����2
B����3
C����4
D����5
�ο��𰸣�B
�����������Ŀ��ָ������ԭ��Ԫ����Cr����õ��ӵ����ʱ���K2Cr2O7��ʧ���ӵ�����һ����Na2SO3������SԪ�صĻ��ϼ۴ӣ�4����6����CrԪ�صĻ��ϼ۽��ӣ�6����n(�軯�ϼ�Ϊn)������������ԭ��Ӧ�е�ʧ�����غ���ɣ���0.05 mol��L��1��0.024 L��(6��4)��0.02 mol��L��1��0.020 L��2��(6��n)�����n��3��
�����Ѷȣ�һ��
5������� д�����л�ѧ��Ӧ����ʽ��
��1����������Һ��ͨ��CO2______
��2��������״�����������Ӧ______
��3��ʵ��������ϩ______��
�ο��𰸣���1��̼������Աȱ��ӵ�����ǿ�����Ա�����ͨ�������̼���ɱ�
���������
�����Ѷȣ���