微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 下面是常见的电化学装置图,①③④中均为惰性电极,下列说法正确的是
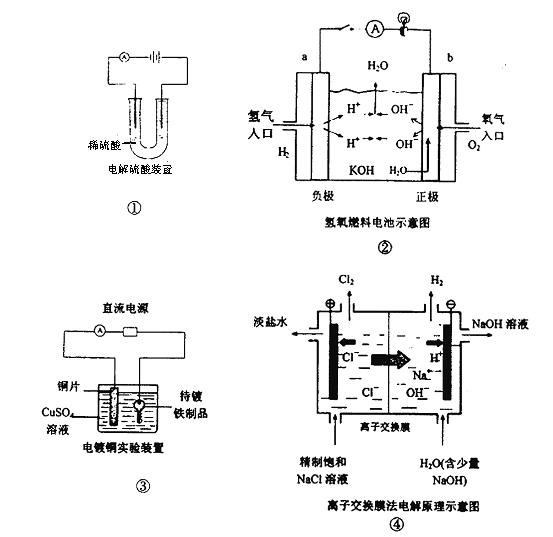
A.装置①中电解一段时间后,溶液的PH不变。
B.装置②中b极为正极,该极的电极反应方程式为O2+4H++ 4e-=2H2O
C.装置③中铜片为阳极,若铜片和铁制品的质量相等,电解一段时间后,电路中有2mol
电子转移,此时铜片和铁制品的质量差为128g
D.装置④中阳离子交换膜上每透过1mol Na+时,则阴极上产生11.2L H2
参考答案:C
本题解析:A项,电解稀硫酸实质是电解水,电解过程中,硫酸的物质的量不变,溶液的体积减少,H+的浓度增大,溶液的PH减少;B项,该电池的电解质溶液为KOH溶液,故该极的电极反应式应为O2+2H2O+4e-=4OH-;C项,阴极反应式:Cu2++2e-="Cu" ,即2mol电子转移时铜片质量增加64克,阳极反应式:Cu-2e-= Cu2+,当2mol电子转移时,铜片质量减少64克,故铜片和铁制品的质量差为128g。D项,阳离子交换膜上每透过1mol Na+时,电子转移1mol,据阴极反应式:2H+ + 2e-+ =H
本题难度:一般
2、选择题 向水中加入等物质的量Ag+、Na+、Pb2+、Cl-、SO42-、NO3-,用惰性电极电解所得溶液,一段时间后氧化产物与还原产物物质的量之比为
A.8∶1
B.2∶1
C.1∶1
D.1∶2
参考答案:D
本题解析:
试题分析:向水中加入等物质的量的Ag+、Na+、Pb2+、Cl-、SO42-、NO3-,发生反应Ag++Cl-=AgCl↓、Pb2++SO42-=PbSO4 ↓,所以混合溶液中只有Na+、NO3-,电解该溶液,实际上是电解水,则一段时间后氧化产物(氧气)与还原产物(氢气)物质的量之比为 1:2,选 D。
考点:考查电解的计算。
本题难度:一般
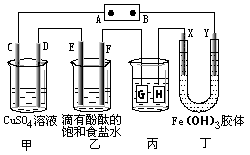
3、填空题 如下图装置所示,C、D、E、F、X、Y都是惰性电极,甲、乙中溶液的体积和浓度都相同(假设通电前后溶液体积不变),A、B为外接直流电源的两极。将直流电源接通后,F极附近呈红色。
请回答:
(1)B极是电源的___________ ,一段时间后,甲中溶液颜色 __________,丁中X极附近的颜色逐渐变浅,Y极附近的颜色逐渐变深,这表明___________ ,在电场作用下向Y极移动。
(2)若甲、乙装置中的C、D、E、F电极均只有一种单质生成时,对应单质的物质的量之比为 ______________。
(3)现用丙装置给铜件镀银,则H应该是______________ (填“镀层金属”或“镀件”),电镀液是___________ 溶液。当乙中溶液的pH是13时(此时乙溶液体积为500mL),丙中镀件上析出银的质量为_____________ ,甲中溶液的pH _____________(填“变大”、“变小”或“不变”)。
(4)若将C电极换为铁,其他装置都不变,则甲中发生总反应的离子方程式是______________ 。
参考答案:(1)负极; 逐渐变浅; 氢氧化铁胶体粒子带正电荷?
本题解析:
本题难度:一般
4、选择题 在1 LK2SO4和CuSO4的混合溶液中,c(SO42-)=2.0 mol・L-1,用石墨作电极电解此溶液,当通电一段时间后,两极均收集到22.4 L(标况)气体,则原溶液中K+的物质的量浓度为??????????????????(???)
A.2.0 mol・L-1
B.1.5 mol・L-1
C.1.0mol・L-1
D.0.5 mol・L-1
参考答案:A
本题解析:略
本题难度:一般
5、选择题 将含有0.4molCu(NO3)2和0.4molKCl的水溶液1L用惰性电极电解一段时间后,在一个电极上析出0.3molCu,此时在另?一个电极上放出气体的体积(标准状况)约为(????)。
A.5 .6L
B.6.72L
C.2.8L
D.13.44L
参考答案:A
本题解析:
试题分析:在阴极析出0.3molCu,则电路中转移了0.6mol电子。阳极有0.4molCl-失电子,失去0.4mol电子,产生0.2molCl2,另外还有0.2mol电子是OH-失去的,产生0.05molO2,因此一共产生标准状况下的气体5.6L,A正确。
点评:考查电解池的原理,具有一定的难度,侧重考查学生的逻辑推理能力和分析问题的能力,解题的关键是找出电极反应得失电子的情况,从而准确解答。
本题难度:简单