微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、填空题 一定量的液态化合物XY2,在一定量O2中恰好完全反应:XY2(l)+3O2(g)====XO2(g)+2YO2(g),冷却后在标准状况下,测得生成物的体积为672 mL,密度为2.56 g・L-1,则
(1)反应前O2的体积为______________________。
(2)化合物XY2的摩尔质量是_____________________。
(3)在XY2分子中,X、Y两元素质量比为3∶16,则X、Y两元素分别为_____________________和_____________________。(写元素名称)
参考答案:(1)672 mL (2)76 g・ mol-1(3)碳硫
本题解析:(1)此反应为反应前后气体体积没有发生改变的反应,而反应前只有O2,所以应该和反应后气体的体积相等为672 mL。(2)根据质量守恒及化学方程式就可以求出参加反应的化合物XY2的质量为0.76 g,物质的量为0.01 mol,从而求出它的摩尔质量。(3)摩尔质量有了,X、Y原子个数之比为1∶2,再根据X与Y的质量比为3∶16,即可求出X和Y的摩尔质量,即X为碳,Y为硫。
本题难度:简单
2、简答题 右图为实验室某盐酸试剂瓶的标签上的有关数据,试回答下列问题:
(1)计算该盐酸中HCl的物质的量浓度;
(2)实验室需要1.19mol/L盐酸20mL,计算所需上述盐酸的体积.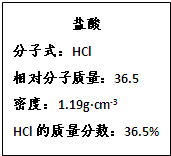
参考答案:(1)该盐酸的物质的量浓度=
本题解析:
本题难度:一般
3、填空题 (6分)实验室欲配制500mL 0.5mol/L的NaOH溶液,有以下仪器:
(1)实验中需要称量NaOH 固体的质量是 。
(2)配制溶液时,一般可以分为以下几个步骤:
①称量 ②计算 ③溶解 ④摇匀 ⑤转移 ⑥洗涤 ⑦定容 ⑧冷却
其正确的操作顺序为(填序号)____________________________。
(3)在配制过程中,如果没有洗涤烧杯和玻璃棒,其他操作都正确的,那么所配溶液的实际浓度将 (填大于、小于或等于)0.5mol/L 。
参考答案:10.0g &
本题解析:
试题分析:(1)氢氧化钠固体的质量为0.5Lx0.5mol/L=0.25mol,故质量m=nM=0.25molx40g/mol=10.0g;(2)配制0.5mol?L-1的NaOH溶液500mL,配制步骤有计算、称量、溶解、移液、洗涤移液、定容、摇匀等操作,用天平称量NaOH(用到药匙),在烧杯中稀释,并用玻璃棒搅拌,加速溶解,冷却后转移到500mL容量瓶中,并用玻璃棒引流,洗涤2-3次,并将洗涤液移入容量瓶,当加水至液面距离刻度线1~2cm时,改用胶头滴管滴加,最后定容颠倒摇匀.所以操作顺序是②①③⑧⑤⑥⑦④.(3)若未洗涤试管和烧杯,则溶质的质量偏少,浓度将会降低,故答案为10.0g ; ②①③⑧⑤⑥⑦④; 小于
考点:物质的量浓度
本题难度:一般
4、选择题 用NA表示阿伏伽德罗常数的数值,下列叙述中错误的是(???)
A.标准状况下,22.4LCH4中含有4 NA个共价键
B.在熔融状态下,1molNaHSO4完全电离出的离子总数为3NA
C.5.5g超重水(T2O)中含有的中子数为3 NA
D.7.8gNa2O2与过量CO2反应,转移电子数为0.1NA
参考答案:B
本题解析:
试题分析:标准状况下,22.4L甲烷的物质的量是1mol,含有4mol共价键,A正确;在熔融状态下,硫酸氢钠的电离方程式是NaHSO4=Na++HSO4-,1molNaHSO4完全电离出的离子总数为2NA,B不正确;超重水含有12个中子,则5.5g超重水(T2O)中含有的中子的物质的量是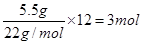 ,C正确;过氧化
,C正确;过氧化
本题难度:一般
5、选择题 1mol/L的Na2SO4溶液是( )
A.溶液中含有1molNa2SO4
B.1升水中加入142gNa2SO4
C.1molNa2SO4溶于1mol水中
D.将322gNa2SO4?10H2O溶于少量水后再稀释成1000mL
参考答案:A、溶液中溶质的物质的量与溶液体积有关,溶液体积未给出,无法
本题解析:
本题难度:简单