微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、实验题 氯化铜是一种广泛用于生产颜料、木材防腐剂等的化工产品。某研究小组用粗铜(含杂质Fe)按下述流程制备氯化铜晶体(CuCl2・2H2O)。

(1)实验室采用如下图所示的装置,可将粗铜与Cl2反应转化为固体1(部分仪器和夹持装置已略去)。
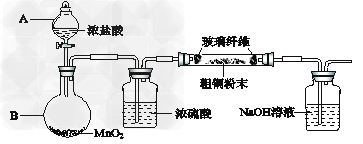
①仪器A的名称是_______________。
②?装置B中发生反应的离子方程是_____________?。
③?有同学认为应在浓硫酸洗气瓶前增加吸收HCl的装置,你认为是否必要(填“是”或“否”)____________。
(2)试剂X用于调节pH以除去杂质,?X可选用下列试剂中的(填序号)__________。
a.NaOH???b.NH3・H2O???c.CuO???d.Cu2(OH)?2CO3???e.CuSO4
(3)在溶液2转化为CuCl2・2H2O的操作过程中,发现溶液颜色由蓝色变为绿色。小组同学欲探究其原因。
已知:在氯化铜溶液中有如下转化关系:
Cu(H2O)42+ (aq)?+4Cl-(aq)?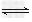 CuCl42-(aq)?+4H2O(l)?
CuCl42-(aq)?+4H2O(l)?
蓝色 黄色
①?上述反应的化学平衡常数表达式是K=?_____________。若增大氯离子浓度,K值(填“增大”、“减小”或“不变”)??????。
②?取氯化铜晶体配制成蓝绿色溶液Y,进行如下实验,其中能够证明CuCl2溶液中有上述转化关系的是(填序号)_____________。
a.将Y稀释,发现溶液呈蓝色
b.在Y中加入CuCl2晶体,溶液变为绿色
c.在Y中加入NaCl固体,溶液变为绿色
d.取Y进行电解,溶液颜色最终消失
参考答案:(1)①分液漏斗????;②MnO2?+4H++2Cl-
本题解析:
本题难度:一般
2、实验题 (二选一)【实验化学】
呋喃甲醇和呋喃甲酸是有机合成中的常用试剂,可用呋喃甲醛制备,其实验原理为:??
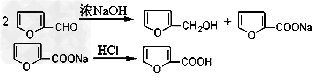
制备方法如下:
①在50mL烧杯中放置3.28mL(0.04mol)呋喃甲醛,并用冰水冷却;称取1.6gNaOH溶于少量水中,在搅拌下滴加氢氧化钠水溶液于呋喃甲醛中。
②在8~12℃下连续搅拌40min。
③向反应混合物加入适量水使其恰好完全溶解,用乙醚萃取分液。
④乙醚萃取物用无水硫酸镁干燥后,先在水浴中蒸去乙醚,然后蒸馏,收集169~172℃馏分得1.4g产品。
⑤在乙醚提取后的水溶液中慢慢滴加浓盐酸到pH=3,搅拌,冷却,结晶,抽滤。
⑥产物用少量冷水洗涤,抽干后,收集粗产物。再提纯后得精产品1.5g。
(1)本实验中,氢氧化钠必须溶于少量的水,否则水量过大主要会影响__________收率。
(2)本实验中要充分连续搅拌40min,其目的是____________________。
(3)萃取时,用到的主要硅酸盐质的仪器是_____________;抽滤的优点是__________。
(4)呋喃甲酸粗产品提纯的方法是______________。
(5)本实验中呋喃甲酸的产率为_____________________。
参考答案:(1)呋喃甲酸
(2)这是在两相中进行的反应,长时间充
本题解析:
本题难度:一般
3、填空题 对硝基甲苯是医药、染料等工业的一种重要有机中间体,它常以浓硝酸为硝化剂,浓硫酸为催化剂,通过甲苯的硝化反应制备。
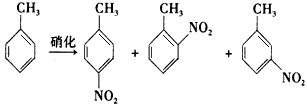
一种新的制备对硝基甲苯的实验方法是:以发烟硝酸为硝化剂,固体NaHSO4为催化剂(可循环使用),在CCl4溶液中,加入乙酸酐(有脱水作用),45℃反应1h。反应结束后,过滤,滤液分别用5%
NaHCO3,溶液、水洗至中性,再经分离提纯得到对硝基甲苯。
(1)上述实验中过滤的目的是____________。
(2)滤液在分液漏斗中洗涤静置后,有机层处于____(填 “上”或“下”)层;放液时,若发现液体流不下来,其可能原因除分液漏斗活塞堵塞外,还有____________________。
(3)下列给出了催化剂种类及用量对甲苯硝化反应影响的实验结果。
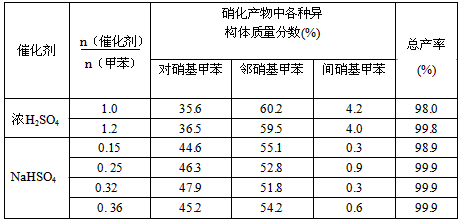
①NaHSO4催化制备对硝基甲苯时,催化剂与甲苯的最佳物质的量之比为________。
②由甲苯硝化得到的各种产物的含量可知,甲苯硝化反应的特点是________________。
③与浓硫酸催化甲苯硝化相比,NaHSO4催化甲苯硝化的优点有________、________。
参考答案:(1)回收NaHSO4
(2)下;分液漏斗上面塞子未
本题解析:
本题难度:困难
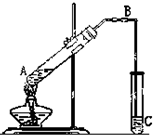
4、简答题 脂类化合物在日常生活中的应用越来越广泛.下图是实验制备乙酸乙酯的装置图,请填写下列空白
(1)试管A中加入无水冰醋酸,但加热后得不到乙酸乙酯,原因是______.(2)导管B的作用______.
(3)试管C中的试剂是______,玻璃导管不能插在液面下,原因是______
(4)要将乙酸乙酯从C中混和物中分离出来的方法是______,必须用到的玻璃仪器是______;
(5)试管A中发生反应的化学方程式为:______.
参考答案:(1)乙酸乙酯的制备反应,反应原料为乙酸和乙醇,浓硫酸起催化
本题解析:
本题难度:简单
5、简答题 溴乙烷是一种重要的有机化工原料,制备溴乙烷的原料有95%乙醇、80%硫酸(用蒸馏水稀释浓硫酸)、研细的溴化钠粉末和几粒碎瓷片,该反应的原理如下:
NaBr+H2SO4→NaHSO4+HBr
CH3CH2OH+HBr
硫酸
CH3CH2Br+H2O
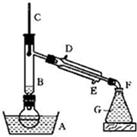
某课外小组欲在实验室制备溴乙烷的装置如图.数据如表.
物质
数据 | 乙醇 | 溴乙烷 | 1,2-二溴乙烷 | 乙醚 | 浓硫酸
密度/g?cm-3
0.79
1.46
2.2
0.71
1.84
熔点(℃)
-130
-119
9
-116
10
沸点(℃)
78.5
38.4
132
34.6
338
在水中的溶解度(g/100g水)
互溶
0.914
1
7.5
互溶
请回答下列问题.
(1)加入药品之前须做的操作是:______,实验进行的途中若发现未加入碎瓷片,其处理的方法是______.
(2)装置B的作用是除了使溴乙烷馏出,还有一个目的是______.温度计的温度应控制在______之间.
(3)反应时有可能生成SO2和一种红棕色气体,可选择氢氧化钠溶液除去该气体,有关的离子方程式是______,______,此操作可在______(填写玻璃仪器名称)中进行,同时进行分离.
(4)实验中采用80%硫酸,而不能用98%浓硫酸,一方面是为了减少副反应,另一方面是为了______.
(5)粗产品中含有的主要有机液体杂质是______,为进一步制得纯净的溴乙烷,对粗产品进行水洗涤、分液,再加入无水CaCl2,进行______操作.
参考答案:(1)实验室制备溴乙烷,用95%乙醇、80%硫酸(用蒸馏水稀
本题解析:
本题难度:简单
|