微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 半导体工业用石英砂做原料通过三个重要反应生产单质硅
①SiO2(s)+2C(s)=Si(s) +2CO(g) △H= +682.44 kJ・mol-1
(石英砂)???? (粗硅)
②Si(s)+2Cl2(g)=SiCl4(g) △H=-657. 01 kJ・mol -1
③SiCl4(g)+2Mg(s) =2MgCl2(s)+Si(s) (纯硅) △H= -625.63 kJ・mol-1
生产1. 00 kg纯硅的总反应热为
[???? ]
A. 2.43×104 kJ
B.-2. 35×104 kJ
C.- 2.23×104kJ
D.-2. 14×104 kJ
参考答案:D
本题解析:
本题难度:一般
2、选择题 在相同温度下,下列三个热化学方程式中Q值的关系是( )
(1)2H2(g)+O2(g)→2H2O(g)+Q1
(2)2H2(g)+O2(g)→2H2O(l)+Q2
(3)H2(g)+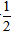 O2(g)→H2O(g)+Q3.
O2(g)→H2O(g)+Q3.
A.Q1>Q2=Q3
B.Q1=Q2=Q3
C.Q2>Q1=2Q3
D.Q1=Q3=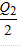
参考答案:C
本题解析:
本题难度:一般
3、选择题
已知使36g焦炭发生不完全燃烧,所得气体中CO占1/3体积,CO2占2/3体积,已知:
C(s)+1/2O2(g)= CO(g) △H =-Q1kJ/mol
CO(g)+1/2O2(g)= CO2(g)△H =-Q2kJ/mol
与这些焦炭完全燃烧相比较,损失的热量是中正确的是
[???? ]
A.1/2Q2 kJ
B.Q2 kJ
C.1/3(Q1+Q2)kJ
D.1/3Q1 kJ
参考答案:B
本题解析:
本题难度:一般
4、选择题 已知:2H2(g)+O2(g)==2H2O(l) ΔH=-571.6 kJ・mol-1 CH4(g)+2O2(g)==CO2(g)+2H2O(l) ΔH=-890kJ・mol-1 现有H2与CH4的混合气体112 L(标准状况),使其完全燃烧生成CO2和H2O(l),若实验测得反应放热3695kJ,则原混合气体中H2与CH4的物质的量之比为
[???? ]
A.1∶1
B.1∶3
C.1∶4
D.2∶3
参考答案:B
本题解析:
本题难度:一般
5、选择题 下列过程属于放热反应的是
A.在生石灰中加水
B.硝酸铵溶于水
C.浓硫酸加水稀释
D.用石灰石煅烧石灰
参考答案:A
本题解析:硝酸铵溶于水、浓硫酸加水稀释都是物理变化,而非化学变化。依据常识,生石灰中加水是放热反应,而石灰石煅烧石灰需要持续高温,故为吸热反应。
本题难度:一般