微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、简答题 锌、碳酸钙、氧气、盐酸、硫酸铜溶液五种物质中选出1种或2种为反应物,按下列反应类型各写1个化学方程式:
(1)化合反应______;
(2)分解反应______;
(3)置换反应______;
(4)复分解反应______.
参考答案:(1)化合反应是由两种或两种以上的物质生成另一种物质的化学反
本题解析:
本题难度:一般
2、计算题 (15分)用KMnO4氧化溶质质量分数为36.5%的盐酸。反应方程式如下:
2KMnO4+16HCl =2KCl+2MnCl 2+5Cl 2↑+8H2O
(1)若此盐酸的密度为1.2g/cm3,其物质的量浓度为
(2)用双线桥表示电子的得失
(3)此反应中氧化剂是 ,氧化产物
(4)若有x mol KMnO4参加反应,则转移电子的物质的量为
(5)15.8g KMnO4完全反应,产生标准状况下Cl2的体积为 ,同时有 mol HCl被氧化。
参考答案:(1)若此盐酸的密度为1.2g/cm3,其物质的量浓度为12
本题解析:
试题分析:(1)根据质量分数与物质的量浓度的换算公式得c=1000×密度×质量分数÷摩尔质量=1000×1.2×36.5%÷36.5=12mol/L。(2)在反应中锰元素化合价降低5价,得到的电子数为2×5,氯元素升高1价,失去的电子数为10×1,标出反应中的得失电子数。(3)反应中高锰酸钾中锰元素化合价降低,故为氧化剂,氯化氢中氯元素化合价升高到氯气,故氯气为氧化产物。(4)根据锰的化合价的变化可以知道,当有xmol KMnO4参加反应,则转移电子的数目为5x mol。(5)15.8g KMnO4为15.8÷158=0.1摩尔,根据反应方程式,完全反应产生Cl20.25摩尔,标准状况下体积为5.6L,同时有0.5 mol HCl被氧化。
考点:质量分数与物质的量浓度的换算,氯气的实验室制法,氧化还原反应中的转移电子数的计算。
本题难度:一般
3、选择题 四种基本类型反应与氧化还原反应的关系可用下列哪个图所示 (??)????
 ???
???
A?????????????????? B?????????????????? C?????????????????? D
参考答案:B
本题解析:
试题分析:首先复分解反应不涉及价态的改变,所以不包含在氧化还原反应中,排除C,置换反应中有新单质生成,涉及到了价态的改变,所以包含在氧化还原反应中,排除A,分解反应与化合反应有的是氧化还原,有的不是,所以B正确。
点评:本题实际上在考查氧化还原反应的本质,是电子的得失,表现为价态的变化,在四种基本反应中,置换反应价态发生改变,复分解反应不改变,化合与分解不一定发生改变。
本题难度:简单
4、选择题 Cl2是纺织工业中常用的漂白剂,Na2S2O3可作为漂白布匹后的“脱氯剂”, S2O32-与Cl2反应的产物之一为SO42一。下列说法中,错误的是 ( )
A.该反应中的氧化剂是C12
B.SO2与氯水的漂白原理相同,所以可用S02做纺织工业的漂白剂
C.上述反应中,每生成1 mol SO42一,可脱去2 mol C12
D.根据该反应可判断还原性:S2O32->C1―
参考答案:B
本题解析:
试题分析:A、Cl元素的化合价降低,则该反应中的氧化剂是Cl2,故A正确;B、二氧化硫漂白是与有色物质化合生成无色物质,而氯水漂白是利用强氧化性,原理不同,故B错误;C、由S2O32-+4Cl2+10OH-=2SO42-+8Cl-+5H2O可知,每生成1mol SO42-,可脱去2mol Cl2,故C正确;D、由还原剂的还原性大于还原产物的还原性可知,还原性:S2O32->Cl-,故D正确;故选B。
考点:考查氧化还原反应的有关判断
本题难度:一般
5、选择题 芯片是电脑、“智能”加点的核心部件,它是用高纯度硅制成的。下面是生产单质硅过程中的一个重要反应:SiO2 + 2C ="===" Si +2CO↑,该反应的基本类型是
A.化合反应
B.分解反应
C.置换反应
D.复分解反应
参考答案:C
本题解析:
正确答案:C
SiO2 + 2C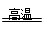 Si +2CO是化合物+单质=化合物+单质的反应,是置换反应,C正确。
Si +2CO是化合物+单质=化合物+单质的反应,是置换反应,C正确。
本题难度:简单