微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 硫酸工业生产应考虑综合经济效益问题。
(1)若从下列四个城市中选择一 处新建一座硫酸厂,你认为厂址宜选在???????????的郊区(填选项的标号)
处新建一座硫酸厂,你认为厂址宜选在???????????的郊区(填选项的标号)
A.有丰富黄铁矿资源的城市
B.风光秀丽的旅游城市
C.消耗硫酸甚多的工业城市
D.人口稠密的文化、商业中心城市
(2)据测算,接触法制硫酸过程中,若反应热都未被利用,则每生产1t 98%硫酸需消耗3.6×105kJ能量。请通过计算判断,若反应:SO2(g)+1/2O2(g) ?SO3(g);△H=-98.3kJ・mol-1;放出的热量能在生产过程中得到充分利用,则每生产1t98%硫酸只需外界提供(或可向外界输出)??????????千焦能量;
(3)CuFeS2是黄铁矿的另一成分,煅烧时,CuFeS2转化为CuO、Fe2O3和SO2,该反应的化学方程式为??????????????????????????????????????????????。
(4)由硫酸厂沸腾炉排出的矿渣中含有Fe2O3、CuO、CuSO4(由CuO与SO3在沸腾炉中化合而成),其中硫酸铜的质量分数随沸腾炉温度不同而变化(见下表)
沸腾炉温度/℃
| 600
| 620
| 640
| 660
|
矿渣中CuSO4的质量分数/%
| 9.3
| 9.2
| 9.0
| 8.4
已知CuSO4在低于660℃时不会分解,请简要分析上表中CuSO4的质量分数随温度升高而降低的原因?????????????????????????????????????????。
参考答案:(1)C(2)输出6.23×105kJ能量
(3)4C
本题解析:略
本题难度:一般
2、选择题 按照绿色化学的原则,最理想的“原子经济”就是反应物的原子全部转化为期望的最终产物,即原子利用率为100%.以下反应不符合这种理念的是( ? ) A.制环氧乙烷:2CH2=CH2+O2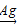 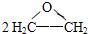
B.制甲基丙烯酸甲酯:CH3C≡CH+CO+CH3OH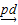 CH2=C(CH3)COOCH3 CH2=C(CH3)COOCH3
C.制丙烯腈:2CH3-CH=CH2+2NH3+3O2→2CH2=CH-CN+6H2O
D.制聚氯乙烯:n?CH2=CHCl 「CH2-CHCl」n 「CH2-CHCl」n
参考答案:C
本题解析:
本题难度:一般
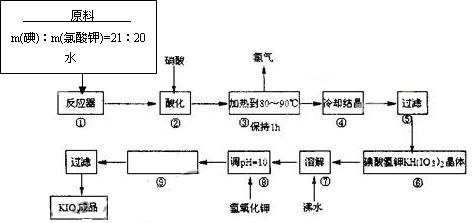
3、填空题
⑴配平反应器中发生的反应方程式:
I2 + ???KIO3 + ???H2O="=" ???KH(IO3)2 + ???KCl + ???Cl2↑
⑵步骤②中,用硝酸而不用HI,其原因可能是????????????????????????????????????
⑶步骤③要保持溶液微沸1小时,以完全排出氯气,排出氯气的原因为?????????????????
?????????????????????????????????????????????????????????????????????????????
⑷合成实验中涉及两次过滤,在实验室进行过滤实验时,用到的玻璃仪器有???????????
⑸用氢氧化钾调节溶液的PH值,发生的反应方程式为:
????????????????????????????????????????????????????????????????????????????
⑹参照碘酸钾溶解度曲线,步骤得到碘酸钾晶体,你建议的方法是?????????????????????
温度
| 0
| 10
| 20
| 40
| 60
| 80
| KIO3g/100g水
| 4.60
| 6.27
| 8.08
| 12.6
| 18.3
| 24.8
参考答案:(每空2分)(1)6,11,3=6,5,3;(2)HI具有还
本题解析:该题以KIO3制备实验为载体,考查了氧化还原反应及其方程式配平,过滤实验的仪器、物质的分离方法等。图、表结合,考查学生的阅读理解能力。(1)略(2)HI有较强还原性,IO3-有较强氧化性,二者发生反应:5I-+IO3-+6H+==3I2+3H2O,所以不能用HI酸化;(3)因为ClO-有强氧化性能将KIO3氧化成KIO4,故在加KOH之前要予以排除。(4)、(5)略(6)由表中数据可知KIO3在常温下的溶解度较小,又KIO3在650℃即分解,故最好采用蒸发浓缩溶液,让KIO3结晶析出再行过滤分离的方法。
本题难度:一般
4、选择题 下列说法一定正确的是(???)
A.氯碱工业中若阳极产生0.1mol氯气则通过溶液的电子的物质的量为0.2mol
B.1L 1mol/LNa2CO3溶液中阴离子和阳离子的总数为3×6.02×1023
C.当碳酸溶液的PH增大1时,溶液中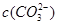 可能增大也可能减小 可能增大也可能减小
D.乙烯和苯分子中都存在碳碳双键,都能发生加成反应
参考答案:C
本题解析:电化学中电子只能在导线中传递,而不能在溶液中,A不正确。碳酸钠水解显碱性,应用消耗1mol碳酸钠产生1mol碳酸氢钠和1mol氢氧化钠,所以溶液中阴离子和阳离子的总数大于3×6.02×1023,B不正确。碳酸的酸性增强,其电离平衡可能被抑制,也可能被促进,C增强。苯分子中不存在碳碳双键,D不正确,答案选C。
本题难度:简单
5、选择题 下列符合化学实验“绿色化学”的有( )
①在萃取操作的演示实验中,将CCl4萃取溴水改为CCl4萃取碘水
②在铜和浓硝酸反应的实验中,将铜片改为可调节高度的铜丝
③将实验室的废酸液和废碱液中和后再排放.
A.①②
B.①③
C.②③
D.①②③
参考答案:D
本题解析:
本题难度:一般
|
|
网站客服QQ: 960335752 - 14613519 - 791315772