��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1��ѡ���� ��֪����1��Zn��s����1/2O2��g��=ZnO��s�� ��H����348��3kJ��mol-1
2Ag��s����1/2O2��g��=Ag2O(s) ��H����31��0kJ��mol-1
��Zn��s����Ag2O��s����ZnO��s����2Ag��s���ġ�H����[???? ]
A����317��3kJ��mol-1
B����379��3kJ��mol-1
C����332��8kJ��mol-1
D����317��3kJ��mol-1
2������� ��֪��Ӧ��CO��g��+H2O��g��?H2��g��+CO2��g����H=-41.2kJ/mol�����ɵ�CO2��H2�Բ�ͬ������Ȼ��ʱ�ں��������µķ�Ӧ���Ƶ�CH4��
��1��850��ʱ��һ���Ϊ10L�ĺ����ܱ������У�ͨ��һ������CO��H2O��g����CO��H2O��g��Ũ�ȱ仯����ͼ��ʾ������˵����ȷ����______������ţ���
A���ﵽƽ��ʱ����Ӧ��ϵ���ջ�ų�49.44kJ����
B����4minʱ����������ƽ����Է����������ٱ仯�����ж��Ѵﵽƽ��
C����6minʱ���������¶ȣ���Ӧƽ�ⳣ��������
D����8minʱ��������CO���ᵼ��v��������v���棩��ƽ��������Ӧ�����ƶ�
��2��850��ʱ�������ݻ�Ϊ2L���ܱ�������ͬʱ����1.0mol?CO��3.0mol?H2O��1.0mol?CO2��x?mol?H2����Ҫʹ������Ӧ��ʼʱ������Ӧ������У���xӦ�����������______��
��3���罫H2?��CO2��4��1������Ȼ�ϣ����ʵ��������¿��Ƶ�CH4����֪��
CH4��g��+2O2��g���TCO2��g��+2H2O��l����H1=-890.3kJ/mol
H2��g��+
1
2
O2��g���TH2O��l����H2=-285.8kJ/mol
��CO2��g����H2��g����Ӧ����CH4��g����Һ̬ˮ���Ȼ�ѧ����ʽ��______��
��4��������ȼ�ϵ����������̼����Ϊ����ʣ���CH4Ϊȼ�ϣ�����Ϊ��������ϡ����������Ϊ�缫��������ӦʽΪ______��������ӦʽΪ______��Ϊ��ʹ��ȼ�ϵ�س�ʱ���ȶ����У���صĵ�������Ӧ�����ȶ���Ϊ�˵�ع���ʱ�����в���A���ʲμ�ѭ������A���ʵĻ�ѧʽ��______��ʵ������У���ͨ���˱�״���¿���448L�����������O2�������Ϊ20%������������ȼ�ϵ�����ı�״����CH4______L��
3������� ��ú��Ϊȼ�Ͽ�ͨ����������;����
;����
C(s)+O2(g)=====CO2(g)����H1��0 ��
;���� ���Ƴ�ˮú����
C(s)+H2O(g)=====CO(g)+H2(g)����H2��0 ��
��ȼ��ˮú����
2CO(g)+O2(g)=====2CO2(g)����H3��0 ��
2H2(g)+O2(g)=====2H2O(g)�� ��H4��0 ��
��ش��������⣺
��1��;����ų�������������_________(����ڡ������ڡ���С�ڡ�);����ų���������
��2����H1����H2����H3����H4����ѧ��ϵʽ��_______________��
��3����֪��
�� C(s)��O2(g)��CO2(g)��??��H��-393��5 kJ��mol-1
�� 2CO(g)��O2(g)��2CO2(g)��??��H��-566 kJ��mol-1
�� TiO2(s)��2Cl2(g)��TiCl4(s)��O2(g)��??��H��+141 kJ��mol-1
��TiO2(s)��2Cl2(g)��2C(s)��TiCl4(s)��2CO(g)�Ħ�H��______________��
��4����֪���и����Ȼ�ѧ����ʽ
��1��Fe2O3(s)+3CO(g)=2Fe(s)+3CO2 ��H=��25kJ/mol
��2��3Fe2O3(s)+CO(g)=2Fe3O4(s)+CO2(g) ��H=��47kJ/mol
��3��Fe3O4(s)+CO(g)=3FeO(s)+CO2(g) ��H=+640kJ/mol
��д��FeO(s)��CO(g)��ԭ��Fe��CO2(g)���Ȼ�ѧ����ʽ________________________��
��5���ڱ�״���µ�11��2L������ȫȼ������CO2��Һ̬ˮ�ų�444��8KJ������298K�������Ȼ�ѧ����ʽΪ___________________��֪��������1mol��ѧ����Ҫ���յ������ֱ�Ϊ��C=O:745KJ/mol��
O=O:496kJ/mol , C-H:414KJ/mol �����1molH-O����Ҫ�ṩ������Ϊ_____________kJ
4��ѡ���� ��֪��
2CO(g)+O2(g)=2CO2(g) ��H= -566 kJ/mol
N2(g)+O2(g) =2NO(g)��H=+180 kJ/mol
��2CO(g)+2NO(g)=N2(g)+ 2CO2(g)�ġ�H��
[???? ]
A.-386 kJ/mol
B. +386 kJ/mol
C.?-746 kJ/mol
D. +746 kJ/mol
5������� ?����̼ѭ������������ĸ߶����ӣ�����ν��ʹ�����CO2�ĺ�������Ч�ؿ�������CO2��������ȫ������ձ����ӡ����ԡ���̼���á�����Ϊ��ѧ���о�����Ҫ����
��1���õ绡���ϳɵĴ�������̼�ܳ����д�����̼�����������ʣ������ֿ������������������ᴿ������ɸ÷�Ӧ�Ļ�ѧ����ʽ��
___?C+?___?KMnO4+?____?H2SO4��____CO2��+?____MnSO4?+?____K2SO4+?____H2O??
��2������ͬ����CO��g����H2O��g���ֱ�ͨ�뵽���Ϊ2L�ĺ����ܱ������У����з�Ӧ
CO��g����H2O��g�� CO2��g����H2��g�����õ������������� CO2��g����H2��g�����õ�������������
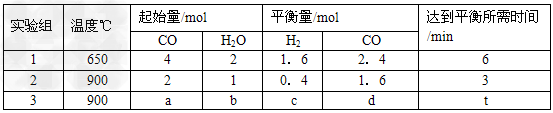
��ʵ��1������ƽ�ⳣ��K=________��ȡС����λ����ͬ����
��ʵ��3�У���ƽ��ʱ��CO��ת���ʴ���ˮ��������a/b?��ֵ_______(�����ֵ��ȡֵ��Χ)��
��ʵ��4����900��ʱ���ڴ������м���10molCO��5molH2O��2molCO2��5molH2�����ʱ
V��______V�棨�<��>��=������
��3����֪�ڳ��³�ѹ�£�
��?2CH3OH(l)?��?3O2(g)?��?2CO2(g)?��?4H2O(g)???��H?��?��1275.6?kJ/mol
��?2CO(g)+?O2(g)?��?2CO2(g)???��H?��?��566.0?kJ/mol
��?H2O(g)?��?H2O(l)???��H?��?��44.0?kJ/mol
д���״�����ȫȼ������һ����̼��Һ̬ˮ���Ȼ�ѧ����ʽ��___________________
��4������п�ѧ��������룺�ѿ�������̼�����Һ��Ȼ���ٰ�CO2����Һ����ȡ����������ѧ��Ӧ��ʹ֮��Ϊ������ȼ�ϼ״����ù��뼼���������£�
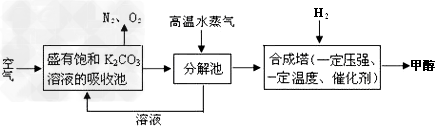
��ֽ����ͨ�����ˮ������������_______________________________?????
��5��CO2����Ȼ��ѭ��ʱ����CaCO3��Ӧ��CaCO3��һ���������ʣ���Ksp=2.8��10-9��
CaCl2��Һ��Na2CO3��Һ��Ͽ��γ�CaCO3�������ֽ��������CaCl2��Һ��Na2CO3��Һ��ϣ���Na2CO3��Һ��Ũ��Ϊ2��10-4mo1/L?�������ɳ�������CaCl2��Һ����СŨ��Ϊ________________?��
|