微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、实验题 NaClO2的漂白能力是漂白粉的4~5倍, NaClO2广泛用于造纸工业、污水处理等。工业上生产NaClO2的工艺流程如下:
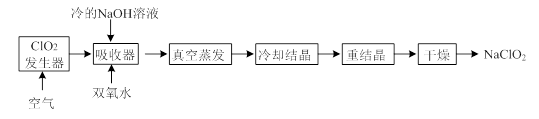
(1)ClO2发生器中的反应为:2NaClO3+SO2+H2SO4=2ClO2+2NaHSO4。实际工业生产中,可用硫磺、浓硫酸代替原料中的SO2,其原因为?????(用化学方程式表示)。
(2)反应结束后,向ClO2发生器中通入一定量空气的目的:?????。
(3)吸收器中生成NaClO2的离子反应方程式为?????,其中反应温度不能高于5℃的可能原因:?????。
(4)某化学兴趣小组用如下图所示装置制备SO2并探究SO2与Na2O2的反应:
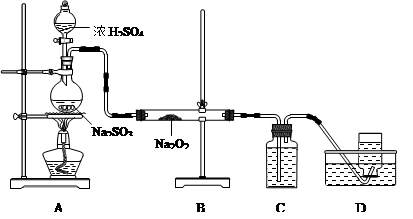
①为除去过量的SO2,C中盛放的试剂为?????。
②D中收集到的气体可使带余烬的木条复燃,B中发生的反应可能为?????、Na2O2+SO2= Na2SO4。
参考答案:
(1)S+2H2SO4(浓)  本题解析:
本题解析:
试题分析:(1)反应需要SO2,故其它原料也是产生SO2,该原料硫与浓硫酸发生归中反应生成SO2;(2)通入空气是为了排除装置中的气体,使其充分吸收;(3)吸收器飞反应物为氢氧化钠、双氧水和ClO2,产物是NaClO2和双氧水的氧化产物氧气;双氧水不稳定受热分解;(4)①吸收SO2可用碱液吸收;②D装置收集到氧气,故B中反应可能有过氧化钠与二氧化碳反应类似发生歧化反应。
本题难度:一般
2、选择题 下列实验操作、现象和解释都正确的是
选项
| 实验操作
| 现象
| 解释
|
A
| 在密闭容器中加热CuO
| 黑色固体变成红色固体
| CuO受热分解得到单质Cu
|
B
| 将SO2通入品红溶液中
| 溶液褪色
| SO2具有漂白性
|
C
| 将Mg、Al与NaOH溶液组成原电池
| Al电极溶解
| Al比Mg金属活动性强
|
D
| 向某溶液中加入盐酸酸化的氯化钡溶液
| 有白色沉淀生成
| 该溶液中一定含有SO42-
参考答案:B
本题解析:CuO受热分解生成了红色的Cu2O和O2,A错误;SO2具有漂白性,能够使品红溶液褪色,B正确;Al比Mg金属活动性弱,在Mg、Al与NaOH溶液组成原电池中,由于Al能够与NaOH溶液反应,而Mg不能,故Al电极溶解,C错误;加入盐酸酸化的氯化钡溶液,产生的白色沉淀可能是BaSO4,也可能是AgCl,故该溶液中可能含有SO42-,也可能含有Ag+,或者既含有SO42-又含有Ag+,D错误。
本题难度:一般
3、选择题 只用下列一种物质不能鉴别:苯、CCl4、KI溶液、NaCl溶液、Na2SO3溶液的是
A.FeCl3溶液
B.AgNO3溶液
C.溴水
D.KMnO4溶液
参考答案:B
本题解析:
试题分析:A.分别混合的现象为:不反应分层后有机层在上层、不反应分层后有机层在下层、溶液变为浅绿色、不反应不分层、生成沉淀和气体,现象不同,能鉴别,故A不符合题意;B、NaCl溶液、Na2SO3溶液与AgNO3溶液均生成白色沉淀,现象相同,不能鉴别,故B正确;C、与溴水分别混合的现象为:不反应分层后有机层在上层、不反应分层后有机层在下层、溶液变为棕黄色、不反应不分层、溴水褪色,现象不同,能鉴别,故C不符合题意;D、分别混合的现象为:不反应分层后有机层在上层、不反应分层后有机层在下层、溶液褪色且溶液变为棕黄色、不反应不分层、溶液褪色,现象不同,能鉴别,故D不符合题意,答案选B。
本题难度:一般
4、选择题 对下列各组物质进行区别的实验方案(见括号内)不妥的是
A.溴水和碘水(淀粉溶液)
B.硫酸铵与氯化铵(采用加碱加热闻其气味的方法)
C.NaCl与KCl(采用灼烧观察焰色的方法)
D.K2CO3与KNO3(采用加盐酸观察其是否有气泡产生的方法)
参考答案:B
本题解析:
试题分析:A、单质碘遇淀粉显蓝色,所以可以用淀粉鉴别溴水和碘水,A正确;B、硫酸铵与氯化铵都是铵盐,都和强碱反应放出氨气,因此不能采用加碱加热闻其气味的方法鉴别硫酸铵和氯化铵,B不正确;C、钠的焰色反应是黄色,钾的焰色反应是紫色(通过蓝色钴玻璃),因此可以通过焰色反应区分氯化钠与氯化钾,C正确;D、碳酸钾与盐酸反应放出CO2,但硝酸钾与盐酸不反应,所以采用加盐酸观察其是否有气泡产生的方法可以鉴别碳酸钾和硝酸钾,D正确,答案选B。
本题难度:一般
5、选择题 下列实验操作正确且能达到预期目的的是
?
| 实验目的
| 操作
| A
| 检验淀粉水解产物有还原性
| 淀粉溶液和稀H2SO4混合加热,冷却后,再加新制的Cu(OH)2悬浊液加热至沸腾
| B
| 证明SO2具有漂白性
| 将SO2通入溴水中
| C
| 为了提取溴水中的溴
| 加入植物油进行萃取
| D
| 浓、稀HNO3分别与Cu反应
| 比较浓、稀HNO3的氧化性强弱
?
参考答案:D
本题解析:A项忽视了应先中和作催化剂的稀H2SO4,错误; SO2使溴水褪色体现了其还原性而非漂白性,B项错误;植物油的主要成分为不饱和高级脂肪酸甘油酯,可以和Br2发生加成反应,C项错误;根据浓、稀硝酸分别与Cu反应的剧烈程度可比较浓、稀HNO3氧化性的强弱,D项正确。
本题难度:一般
|
|