微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、计算题 氨和联氨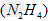 是氮的两种常见化合物。在科学技术和生产中有重要的应用。?根据题意完成下列计算:?
是氮的两种常见化合物。在科学技术和生产中有重要的应用。?根据题意完成下列计算:?
(1)联氨用亚硝酸氧化生成氮的另一种氢化物,该氢化物的相对分子质量为43.0,其中氮原子的质量分数为0.977,计算确定该氢化物的分子式。该氢化物受撞击则完全分解为氮气和氢气。4.30?g该氢化物受撞击后产生的气体在标准状况下的体积为________?L。?
(2)联氨和四氧化二氮可用作火箭推进剂,联氨是燃料,四氧化二氮作氧化剂,反应产物是氮气和水。由联氨和四氧化二氮组成的火箭推进剂完全反应生成72.0?kg水,计算推进剂中联氨的质量。?
(3)氨的水溶液可用于吸收NO与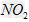 的混合气体,反应方程式为
的混合气体,反应方程式为
?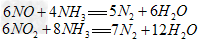
NO与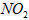 混合气体180?mol被8.90×103g氨水(质量分数0.300)完全吸收,产生156?mol氮气。吸收后氨水密度为0.980?g/cm3。计算:?
混合气体180?mol被8.90×103g氨水(质量分数0.300)完全吸收,产生156?mol氮气。吸收后氨水密度为0.980?g/cm3。计算:?
①该混合气体中NO与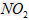 的体积比。?
的体积比。?
②吸收后氨水的物质的量浓度(答案保留一位小数)。?
(4)氨和二氧化碳反应可生成尿素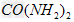 。尿素在一定条件下会失去氨而缩合。如两分子尿素失去一分子氨形成二聚物:?
。尿素在一定条件下会失去氨而缩合。如两分子尿素失去一分子氨形成二聚物:?
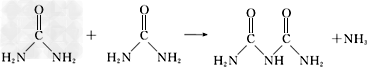
已知常压下120?mol??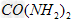 在熔融状态发生缩合反应,失去80?mol??
在熔融状态发生缩合反应,失去80?mol??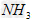 生成二聚物
生成二聚物
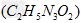 和三聚物。测得缩合产物中二聚物的物质的量分数为0.60,推算缩合产物中各缩合物的物质的量之比。
和三聚物。测得缩合产物中二聚物的物质的量分数为0.60,推算缩合产物中各缩合物的物质的量之比。
参考答案:(1)![]() 本题解析:
本题解析:
本题难度:一般
2、选择题 把一定量的锌与100 mL,18.5mol/L,的浓硫酸充分反应后,锌完全溶解,同时生成气体Y 33.6L(在标准状况下)。将反应后的溶液稀释到l L,测得溶液的pH=1,则下列叙述正确的是 [???? ]
A.气体Y是SO2和H2的混合物
B.气体Y中SO2和H2的体积比为4:1
C.反应中共消耗锌87.5g
D.反应中共转移电子3mol
参考答案:AD
本题解析:
本题难度:一般
3、选择题 1 mol过氧化钠与2 mol碳酸氢钠固体混合后,在密闭容器中加热充分反应,排出气体物质后冷却,残留的固体物质是
[???? ]
A.Na2CO3
B.Na2O2 Na2CO3
C.NaOH Na2CO3
D.Na2O2 NaOH Na2CO3
参考答案:A
本题解析:
本题难度:一般
4、填空题 据报道,目前一些地区酸雨、灰霾和光化学烟雾等区域性大气污染突出,严重威胁群众健康,影响环境 安全。二氧化硫和氮的氧化物是大气的主要污染物,关注臭氧层、防止和治理环境污染是当前环保工作的重要研究内容之一。
(1)汽车尾气主要含有CO2、CO、SO2、NO及汽油、柴油等物质,这种尾气越来越成为城市空气污染的主要来源。汽车尾气中的CO来自_________,NO来自_________。
(2)空气中微量的臭氧对人有益,浓度过大则是一种污染气体,臭氧作为强氧化剂,几乎能与任何生物组织反应。下列有关说法正确的是_________。
A.停止使用氟里昂是为了保护臭氧层
B.光化学烟雾与大气臭氧的生成有关
C.家用电器消毒柜中产生的臭氧能够高效杀菌消毒
D.臭氧能使湿润的碘化钾一淀粉试纸变蓝
(3)一定条件下,2SO2(g)+O2(g)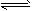 2SO3(g),向2L密闭容器中通入2mol SO2(g)、1mol O2(g)和0.2mol
2SO3(g),向2L密闭容器中通入2mol SO2(g)、1mol O2(g)和0.2mol
SO3(g),2min后反应达到平衡时,测得SO2的转化率为50%,则该可逆反应的平衡常数K=________。
(4)在一定条件下用氨可将氮氧化物转化为无毒气体。同温同压下,3.5 L NH3恰好将3.0 L NO和NO2的混合气体完全转化为N2,原混合气体中NO和NO2的体积比是_________。
(5)新型纳米材料氧缺位铁酸盐(ZnFe2Ox),由铁酸盐(ZnFe2O4)经高温还原制得,常温下,它能将工业废 气中的酸性氧化物分解除去,转化流程如图所示。若2 mol ZnFe2Ox与SO2反应可生成0.75 mol S,则x=
__________。
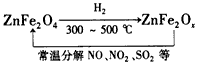
参考答案:(1)汽油的不完全燃烧;N2与O2在汽车气缸内高温环境下的反
本题解析:
本题难度:一般
5、选择题 有10 g不纯CaCO3样品与足量盐酸作用后生成4.44 g CO2,且溶液中残留难溶物质。则对于此样品中是否存在①MgCO3;②K2CO3;③SiO2杂质的判断中,正确的是 [???? ]
A.肯定含①③,不含②
B.肯定含①③,可能含②
C.肯定含②③,不含①
D.肯定含②③,可能含①
参考答案:B
本题解析:
本题难度:一般