��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1������� A��B��C��D��Ϊ��ѧ��ѧ�������ʣ��Һ���һ����ͬ��Ԫ�أ�����֮��������ת����ϵ������A�ǵ��ʡ�

��1����A��һ�ֵ���ɫ���壬B����̬�⻯�C��DΪ��̬�������C���γ��������Ҫ���ʡ���д��C��B��Ӧ�Ļ�ѧ����ʽ_________________________________��
��2����B����̬�⻯�C��DΪ��̬�������C��D���γɹ⻯ѧ������һ����Ҫԭ����д����Ӧ�۵Ļ�ѧ����ʽ____________________________________��ʵ�����м�������B�����õ��Լ�����ƷΪ________________��
��3����B��D��������ǿ����Һ����������ǿ����Һ����Ӧ�ڢ۾���Ҫǿ������Һ����Ӧ�ܿ���ͨ���μ�����ϡ����ʵ�֡��ݴ��ж�AԪ�������ڱ��е�λ����_________________����д���ڵ����ӷ���ʽ_____________________________________________________________________________��
��4����C��һ�ֵ���ɫ���壬��������������еĹ�������D��һ��ǿ�д����Ӧ�ܵ����ӷ���ʽ
_____________________________________________________________________________________��
�ο��𰸣���1��2H2S��SO2��3S��2H2O��2�֣�
��2��
���������
�����������1����A��һ�ֵ���ɫ���壬B����̬�⻯�C��DΪ��̬�������C���γ��������Ҫ���ʣ������������Ӧ����A��S��B��H2S��C��SO2��D��SO3��H2S���л�ԭ�ԣ�SO2���������ԣ����߿��Է���������ԭ��Ӧ���ɵ������ˮ����Ӧ�Ļ�ѧ����ʽΪ2H2S��SO2��3S��2H2O��
��2����B����̬�⻯�C��DΪ��̬�������C��D���γɹ⻯ѧ������һ����Ҫԭ����˵���ǵ�Ԫ�ؼ��仯�����ת�������A�ǵ�����B�ǰ�����C��NO��D��NO2��������������������NO��ˮ�����Է�Ӧ�۵�
�����Ѷȣ�һ��
2������� ��֪����1��A��XY����������Ǻ�ɫ��ĩ����2����A��ϡ���Ṳ�ȣ�����ҺB����B�е������� ��Һ�����ɰ�ɫ���������˺����ҺC����3����C�ֳ����ݣ���һ���м����ռ���Һ���ɵ���ɫ��״����D����4������һ��C�з���һö���������е���E��������֪A��B��C��D��E���ϵ��ͼ��ʾ��
��Һ�����ɰ�ɫ���������˺����ҺC����3����C�ֳ����ݣ���һ���м����ռ���Һ���ɵ���ɫ��״����D����4������һ��C�з���һö���������е���E��������֪A��B��C��D��E���ϵ��ͼ��ʾ��
��1��д��A��B��C��D��E�����ʵĻ�ѧʽ��A__________��B__________��C__________��D__________��E__________��
��2����д��������Ӧ�����ӷ���ʽ��
???????????????????????????????��?????????????????????????????��
???????????????????????????????��?????????????????????????????��
�ο��𰸣�3Fe+2O2 �����������
�����������
�����Ѷȣ���
3���ƶ��� ����A����AԪ����ɵĵ��ʣ������ھƾ��ƻ��������գ����� Ϊ��ɫ��B��C��D�Ǻ���AԪ�ص����� ��ͬ�����A��B��C��D����ͼ��ʾ��ϵ����ת����?

(1)д���������ʵĻ�ѧʽ�� A____��B____��C___��D____��
(2)д���٢ڢ۵����ӷ���ʽ���ܵĻ�ѧ����ʽ�� ��____�� ��___�� ��____�� ��____��
�ο��𰸣�(1)Na ��NaOH ��Na2CO3 ��NaCl
(
���������
�����Ѷȣ�һ��
4���ƶ��� ������ѧ��ѧ�г������ʵ�ת����ϵͼ�У���Ӧ���������ַ�Ӧ��Ͳ���δȫ��ע������֪A��DΪ�������ʣ�����Ϊ���������CΪ������������ƶϣ�
��������ʾ������Al���ڸ����½�һЩ�����������������û�������
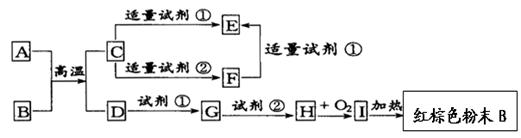
��1��д�����ʵĻ�ѧʽ��
A��???????????B��????????????C��?????????????H��??????????
��2��д�����з�Ӧ�ķ���ʽ��
A��D��Ӧ�Ļ�ѧ����ʽ???????????????????????????????????????????????????
C��F��Ӧ�����ӷ���ʽ????????????????????????????????????????????????
D��G��Ӧ�����ӷ���ʽ????????????????????????????????????????????????
�ο��𰸣���1��
A��?? Al???????? B��?? F
���������
�����������BΪ����ɫ��ĩ��֪��BΪFe2O3�����ת����ϵͼ��֪��IΪFe��OH��3��HΪFe��OH��2��GΪFeCl2��DΪFe��A+B��D+CΪ���ȷ�Ӧ����AΪAl��CΪAl2O3��EΪAlCl3��FΪƫ�����Σ������Լ���Ϊ���ᣬ�Լ���Ϊǿ���NaOH��KOH�ȣ���
��1��������������֪��AΪAl��BΪFe2O3��CΪAl2O3��IΪFe��OH��3���ʴ�Ϊ��Al��Fe2O3��Al2O3��Fe��OH��3������
��2�������Ϸ����������ѧ֪ʶ��д���ӷ���ʽ��
���������⿼��
�����Ѷȣ�һ��
5������� ��13�֣������ڵ�����Ԫ��A��B��C��D��E��ԭ��������������A��B��C����Ԫ��ԭ�Ӻ�����Ӳ���֮����5��A��B��Ԫ��ԭ��������Ӳ��ϵ�����֮�͵���CԪ��ԭ��������Ӳ��ϵĵ�������BԪ��ԭ��������Ӳ��ϵĵ����������ĵ��Ӳ�����2����A��C�����γɻ�����CA3��B��D��ԭ������֮��Ϊ3�U4��Eԭ�������������ȴ�����������1����ش�
��1��E��Ԫ�����ڱ���λ��Ϊ���ߡ���
��2��A��B��C��Dԭ�Ӱ뾶�Ӵ�С��˳��Ϊ���ߡ��ߣ���Ԫ�ط��ţ�
��3����A��B����Ԫ����ɵķ����ж��֣�����һ�ַ��Ӻ�4��ԭ�ӣ��ҷ���Ϊֱ���͵ĶԳƽṹ��д�������ʽ�ߡ��ߡ�
��4������A��B��C��D����Ԫ����ɵ����Σ��ȿ��������ᷴӦ�ֿ�����NaOH�� Һ��Ӧ���仯ѧʽΪ�ߡ��ߡ�
Һ��Ӧ���仯ѧʽΪ�ߡ��ߡ�
��5����A��C��E����Ԫ����ɵĻ�����C2A6E2��һ����Ҫ�Ļ���ԭ�ϣ��������ӻ����������ˮ����Һ�����ԣ�ˮ��ԭ����NH4Cl���ơ�д���û������һ��ˮ�ⷴӦ�����ӷ���ʽ�ߡ��ߡ�
��6����̬��������ҽѧ������Ҫ����;��������Fe3O4�Ǵ������е���Ҫ���ӣ����Ʊ����̼�ʾ���£�
�ٽ�������CA3ͨ������ʵ�����ϵ�FeSO4��Fe2(SO4)3��Һ�У��������ּд���ù��̵������ӷ���ʽ�ߡ��ߡ�
��������Ӧ���ɵ����ּ�������ã��õ�Fe3O4���÷�Ӧ�Ļ�ѧ����ʽΪ�ߡ��ߡ�
�ο��𰸣���13�֣���1���������ڢ�A��?��2��C��N��O��H��3��<
�����������
�����Ѷȣ�һ��