微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、填空题 离子反应是中学化学中重要的反应类型,回答下列问题:
(1)在发生离子反应的反应物或生成物中,一定存在有______(填编号).
①单质??②氧化物??③电解质??④盐??⑤化合物
(2)可用图示的方法表示不同反应类型之间的关系.如分解反应和氧化还原反应可表示为下图.请在下面的方框中画出离子反应、置换反应和氧化还原反应三者之间的关系.

(3)有一瓶澄清的溶液,其中可能含有H+、NH+4、Mg2+、Ba2+、Al3+、I-、NO-3、CO2-3、SO2-4、AlO-2,取该溶液进行以下实验:
①取pH试纸检验,表明溶液呈强酸性.排除______离子存在.
②取出部分溶液,加入少量CCl4及数滴新制氯水,经振荡后CCl4呈紫红色,可以排除______存在.
③另取部分溶液逐渐加入NaOH溶液,使溶液从酸性逐渐变为碱性,在反应过程中均无沉淀产生,则可排除______的存在.
④取部分上述碱性溶液加Na2CO3溶液,有白色沉淀生成,证明______存在,又排除______存在.
⑤根据上述实验事实还不能确定是否存在的离子是______.
参考答案:(1)离子反应是由离子参加的反应,发生的条件是化合物在一定的
本题解析:
本题难度:一般
2、选择题 在NaOH溶液中能大量共存的离子组是
A.NH4+、HCO3-
B.Fe3+、NO3-
C.SiO32-、AlO2-
D.Ca2+、SO42-
参考答案:C
本题解析:
本题难度:一般
3、选择题 锌片与盐酸的反应属于
A.吸热反应
B.放热反应
C.既是吸热反应又是放热反应
D.都不是
参考答案:B
本题解析:金属与酸的反应都是放热反应.
本题难度:简单
4、选择题 下列反应的离子方程式书写错误的是
A.向硫酸亚铁溶液中加入稀硝酸:3Fe2++NO3-+4H+=3Fe3++NO↑+2H2O
B.铜和稀硝酸的反应:Cu+4H++NO3-=Cu2++NO↑+2H2O
C.向氯化铁溶液中加入稀氨水:Fe3++3OH-=Fe(OH)3↓
D.Ba(OH)2和(NH4)2SO4溶液的混合加热:Ba2++2OH-+2NH4++SO42-BaSO4↓+2NH3↑+2H2O
参考答案:BC
本题解析:分析:A、硝酸具有强氧化性,可以加还原性的离子氧化;
B、离子方程式遵循电荷守恒;
C、氨水是弱电解质,不能拆成离子形式;
D、钡离子和硫酸根离子、铵根离子和氢氧根离子在溶液中发生反应.
解答:A、硝酸具有强氧化性,将亚铁离子氧化的方程式为:3Fe2++NO3-+4H+=3Fe3++NO↑+2H2O,故A正确;
B、铜和稀硝酸的反应:3Cu+8H++2NO3-=3Cu2++2NO↑+4H2O,离子方程式遵循电荷守恒,故B错误;
C、氨水是弱电解质,不能拆成离子形式,即Fe3++3NH3?H2O=Fe(OH)3↓+3NH4+,故C错误;
D、Ba(OH)2和(NH4)2SO4溶液的混合加热,钡离子和硫酸根离子、铵根离子和氢氧根离子在溶液中发生反应,即
Ba2++2OH-+2NH4++SO42- BaSO4↓+2NH3↑+2H2O,故D正确.
BaSO4↓+2NH3↑+2H2O,故D正确.
故选BC.
点评:本题考查离子方程式的正误判断,题目难度不大,注意从化学式、离子符号、电荷守恒以及是否符合反应实际的角度分析离子方程式的书写是否正确.
本题难度:困难
5、选择题 1?L某混合溶液中,溶质X、Y浓度都为0.1mol・L-1,向混合溶液中滴加 0.1?mol/L某溶液Z,所得沉淀的物质的量如图所示,则X、Y、Z分别是
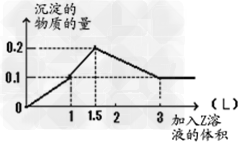 [???? ]
[???? ]
A.偏铝酸钠、氢氧化钡、硫酸????????????
B.氯化铝、氯化镁、氢氧化钠
C.氯化铝、氯化铁、氢氧化钠????????????
D.偏铝酸钠、氯化钡、硫酸
参考答案:A
本题解析:
本题难度:一般