微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 对于反应2SO2(g)+O2(g)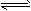 2SO3(g)能增大正反应速率的措施是[???? ]
2SO3(g)能增大正反应速率的措施是[???? ]
A.通入大量O2
B.增大容器容积
C.移去部分SO3
D.降低体系温度
参考答案:A
本题解析:
本题难度:一般
2、选择题 可以证明可逆反应N2(g)+3H2(g)?2NH3(g)已达平衡状态的是( )
①一个N≡N键断裂的同时,有3个H-H键断裂;②一个N≡N键断裂的同时,有6个N-H键断裂;③其他条件不变时,混合气体的总质量不变;④恒温恒容下的反应,体系压强不再改变;⑤反应体系中反应物和生成物的百分含量都不再改变;⑥恒温恒压下的反应,密度不再改变;⑦正反应速率v(H2)=0.6mol/(L?min),逆反应速率v(NH3)=0.4mol/(L?min)
A.全部
B.②④⑤⑥⑦
C.②③④⑤⑥⑦
D.③④⑤⑥⑦
参考答案:①无论是否达到平衡状态,只要一个N≡N断裂的同时,就有3个H
本题解析:
本题难度:简单
3、填空题 研究NO2、、CO等大气污染气体的处理具有重要意义。
利用反应6NO2(g)+8NH3(g)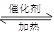 7N2(g)+12 H2O(g)可处理NO2。700℃时,向容积为2L的密闭容器中充入一定量的NO2和NH3, 反应过程中测定的部分数据见下表
7N2(g)+12 H2O(g)可处理NO2。700℃时,向容积为2L的密闭容器中充入一定量的NO2和NH3, 反应过程中测定的部分数据见下表
反应时间/min
| n(NO2)/mol
| n(NH3)/ mol
|
0
| 1.20
| 1.60
|
2
| 0.90
| ?
|
4
| ?
| 0.40
(1)反应在2min内的平均速率为v(NH3)=??????????????,4min该反应达到平衡状态,则该反应的平衡常数K的表达式为????????????,NO2的转化率为????????????
(2)700℃ ,将NO2与NH3以体积比1:2置于密闭容器中发生上述反应,下列能说明反应达到平衡状态的是???????。
a.体系压强保持不变
b.混合气体颜色保持不变
c.体系密度保持不变
d.每消耗1 mol NO2的同时生成2 来源:91考试网 91ExaM.orgmol H2O
参考答案:(1)0.10mol/(L・min)??????C7(N2)
本题解析:
试题分析:由方程式可知反应物和生成物的反应计量数之和不相等所以压强不变时达到平衡状态;混合气体的颜色保持不变也表明达到平衡状态;因为反应物和生成物均为气体,气体的质量不变容器的体积不变所以体系的密度始终不变。
本题难度:一般
4、填空题 (16分)氨气是一种重要的基础化工原料,用途广泛。
(1)在微电子工业中,氨水可作刻蚀剂H2O2的清除剂,产物不污染环境。该反应的化学方程式为2NH3 + 3H2O2= +6H2O
(2)工业中常用以下反应合成氨:N2+3H2 2NH3 △H<0。某实验室在三个不同条件的密闭容器中,分别加入N2和H2,浓度均为c(N2) =" 0.100mol/L," c(H2) = 0.300mol/L,进行反应时, N2的浓度随时间的变化如图①、②、③曲线所示。 2NH3 △H<0。某实验室在三个不同条件的密闭容器中,分别加入N2和H2,浓度均为c(N2) =" 0.100mol/L," c(H2) = 0.300mol/L,进行反应时, N2的浓度随时间的变化如图①、②、③曲线所示。

该反应平衡常数的数学表达式为 ;实验②平衡时H2的转化率为_____ 。
(3)据图所示,②、③两装置中各有一个条件与①不同。请指出,并说明判断的理由。
②条件:_______ 理由: ________
③条件:_______ 理由: ________
参考答案:.(16分)
(1)2NH3 + 3H2O2
本题解析:略
本题难度:一般
5、选择题 2007年国家最高科学技术奖授予石油化工催化剂专家闵恩泽教授,以表彰他在催化剂研究方面做出的突出贡献。下列关于催化剂的说法中正确的是 [???? ]
A.使用催化剂可以增大正反应速率,减小逆反应速率
B.使用催化剂可以提高反应物的转化率
C.使用催化剂可以降低反应的活化能
D.使用催化剂可以改变反应的平衡常数
参考答案:C
本题解析:
本题难度:一般
|