微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 日本地震后,导致福岛第一核电站引发核危机。核反应堆的第一层护罩是锆锡合金外壳,第二层护罩是压力仓,第三层护罩是用最坚固的钢和混凝土制成的非常厚的球体。下列叙述错误的是( )。
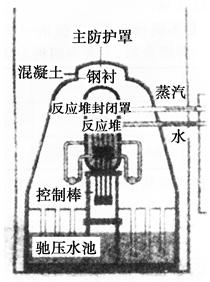
A.锆锡合金、钢、混凝土都属于混合物
B.钢的硬度和熔沸点都高于纯铁
C.锆锡合金和钢属于金属材料,混凝土属于传统的硅酸盐材料
D.在高温下,钢和水蒸气可发生反应产生氢气
参考答案:B
本题解析:钢是铁碳合金,其硬度大于纯铁,但熔点低于纯铁。
本题难度:一般
2、填空题 柠檬酸亚铁(FeC6H6O7)是一种易吸收的高效铁制剂,可由绿矾(FeSO4・7H2O)通过下列反应制备:
FeSO4+Na2CO3=FeCO3+Na2SO4
FeCO3+C6H8O7=FeC6H6O7+CO2+H2O
下表列出了相关金属离子生成氢氧化物沉淀的pH(开始沉淀的pH按金属离子浓度为1.0 mol・L-1计算)。
金属离子
| 开始沉淀的pH
| 沉淀完全的pH
|
Fe3+
| 1.1
| 3.2
|
Al3+
| 3.0
| 5.0
|
Fe2+
| 5.8
| 8.8
?
(1)制备FeCO3时,选用的加料方式是________(填字母),原因是_________________________________
a.将FeSO4溶液与Na2CO3溶液同时加入到反应容器中
b.将FeSO4溶液缓慢加入到盛有Na2CO3溶液的反应容器中
c.将Na2CO3溶液缓慢加入到盛有FeSO4溶液的反应容器中
(2)生成的FeCO3沉淀需经充分洗涤,检验洗涤是否完全的方法是_______________________________。
(3)将制得的FeCO3加入到足量柠檬酸溶液中,再加入少量铁粉,80℃下搅拌反应。
①铁粉的作用是_____________________。
②反应结束后,无需过滤,除去过量铁粉的方法是________________________________。
(4)最后溶液经浓缩、加入适量无水乙醇、静置、过滤、洗涤、干燥,获得柠檬酸亚铁晶体。分离过程中加入无水乙醇的目的是__________________。

(5)某研究性学习小组欲从硫铁矿烧渣(主要成分为Fe2O3、SiO2、Al2O3)出发,先制备绿矾,再合成柠檬酸亚铁。请结合右图的绿矾溶解度曲线,补充完整由硫铁矿烧渣制备FeSO4・7H2O晶体的实验步骤(可选用的试剂:铁粉、稀硫酸和NaOH溶液):向一定量烧渣中加入足量的稀硫酸充分反应,________,得到FeSO4溶液,________,得到FeSO4・7H2O晶体。
参考答案:(1)c 避免生成Fe(OH)2沉淀 (2)取最后一次的洗涤
本题解析:根据题干信息以及FeCO3、Fe2O3、FeSO4的性质解决问题。
(1)根据相关金属离子生成氢氧化物沉淀的pH可知,制备FeCO3时要注意控制溶液的pH。所以需要将Na2CO3缓慢加入到FeSO4溶液中,防止Fe(OH)2的生成。
(2) FeCO3表面吸附SO42―、Na+等杂质离子,检验洗涤是否完全时,可检验SO42―是否存在。方法是取最后一次的洗涤液1~2 mL于试管中,向其中滴加用盐酸酸化的BaCl2溶液,若无白色沉淀产生,则表明已洗涤干净。
(3)Fe2+易被氧化,加入铁粉的
本题难度:困难
3、简答题 某学习小组利用下图所示装置进行“铁与水气反应”和其他实验(略去了夹持仪器).

(1)仪器B的名称是______,石棉绒 的作用是______.
(2)B中发生反应的化学方程式是______.
(3)加热E以前要对装置中的气体验纯,方法是:收集一试管气体,然后______.
(4)已知有反应:Cu20+2H+→Cu+Cu2++H20,则可用来检验反应后E中的红色固体中除Cu外是否含Cu20,可用的试剂是______(填序号)
a.稀硝酸????b.稀硫酸????c.盐酸????d.浓硫酸
(5)在E后若再接二个盛碱石灰的干燥管(依次称为F和G),则还可用该装置测定水的组成或铜的相对原子质量.若反应前盛有药品的E、F的质量分别是bg、cg,反应后分别是dg、eg.
①水中元素的物质的量之比可表示为n(H):n(0)=______;若反应后E中除Cu外还含有另种还原产物Cu20,则该比值将______?(选填“偏大”“偏小”或“无影响”).
②若空的E管的质量为ag,加热后CuO完全还原为Cu,则铜的相对原子质量可表示为______.
参考答案:(1)依据图装置仪器分析,E为固体加热反应的装置,应在硬质玻
本题解析:
本题难度:一般
4、计算题 金属铜能被FeCl3的浓溶液腐蚀,其化学反应是:Cu+2FeCl3=2FeCl2+CuCl2。
 现将有铜的印刷线路板浸入120mLFeCl3的浓溶液中,有9.6gCu被腐蚀掉。取出印刷线路板,向溶液中加入8.4g铁粉,经充分反应,溶液中还存在4.8g不溶物。则: 现将有铜的印刷线路板浸入120mLFeCl3的浓溶液中,有9.6gCu被腐蚀掉。取出印刷线路板,向溶液中加入8.4g铁粉,经充分反应,溶液中还存在4.8g不溶物。则:
 (1)溶液中存在那些离子? (1)溶液中存在那些离子?
 (2)离子的浓度各是多少?(设溶液体积不变) (2)离子的浓度各是多少?(设溶液体积不变)
参考答案:(1)溶液中存在的离子为:Fe2+、Cu2+、Cl-。
本题解析: 存在的不溶物有两种可能:一可能是铁、铜混合物,二可能只是铁。若为铁、铜混合物,则溶液中的Cu2+必然全部析出,即不溶物的质量大于9.6g,显然错误,故不溶物为Cu。 存在的不溶物有两种可能:一可能是铁、铜混合物,二可能只是铁。若为铁、铜混合物,则溶液中的Cu2+必然全部析出,即不溶物的质量大于9.6g,显然错误,故不溶物为Cu。

本题难度:一般
5、选择题 将3.20 g Cu跟10.0 mol/L的硝酸30.0 mL充分反应,还原产物中有NO和NO2 。若反应后溶液中有a mol H+,则此时溶液中NO3- 的物质的量为
A.a/2 mol
B.2a mol
C.0.100 a mol
D.(a + 0.100) mol
参考答案:D
本题解析:
试题分析:由守恒关系可知:铜最终只能转化成硝酸铜,3.20 g Cu的物质的量是0.05mol,所以硝酸铜中的硝酸根是0.1mol。根据氢元素守恒可得,为何铜离子结合的硝酸根是a mol,所以溶液中NO3- 的物质的量为(a + 0.100) mol,故选D。
点评:本题重点考查的是有关硝酸氧化性的知识,考查学生对课本知识的掌握情况和计算能力。
本题难度:简单
|