微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 已知:S(s)+O2(g)→SO2(g)+297.23kJ………………①
2SO2(g)+O2(g)  2SO3(g) +196.64kJ……②
2SO3(g) +196.64kJ……②
假设反应过程中无热量损失,则
A.1mol S(s)完全反应,并转化为SO3(g)时,放出395.55 kJ热量
B.1个SO2和1个O2分子储存的能量之和大于1个SO3分子
C.1 L SO2(g)完全反应生成1L SO3(g),放出98.32 kJ热量
D.使用催化剂,可以减少反应②放出的热量
参考答案:B
本题解析:
试题分析:A、根据盖斯定律可知①×2+②得到2S(s)+3O2(g)→2SO2(g)+791.1kJ,但由于反应②是可逆反应,则1mol S(s)完全反应,并转化为SO3(g)时,放出的热量小于395.55 kJ,A错误;B、反应②是放热反应,则1个SO2和1个O2分子储存的能量之和大于1个SO3分子,B正确;C、系数表示物质的量,则1 mol SO2(g)完全反应生成1mol SO3(g),放出98.32 kJ热量,C错误;D、催化剂不能改变反应热和平衡状态,因此使用催化剂,不能减少反应②放出的热量,D错误,答案选B。
考点:考查反应热的有关计算与判断
本题难度:一般
2、选择题 能用键能大小解释的是
A.N2的化学性质比O2稳定
B.常温常压下,溴呈液态,碘呈固态
C.稀有气体一般很难发生化学反应
D.硝酸易挥发而磷酸难挥发
参考答案:A
本题解析:B、D的性质与分子间作用力有关,C与核外电子的排布有关。
本题难度:简单
3、填空题 (Ⅰ)2SO2(g)+O2(g)  2SO3(g)反应过程的能量变化如图所示。请回答下列问题:
2SO3(g)反应过程的能量变化如图所示。请回答下列问题:
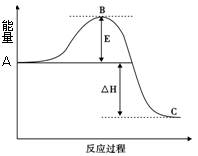
(1)图中A表示 。
(2)E的大小对该反应的焓变有无影响? 。
该反应通常用V2O5作催化剂,加V2O5会使图中B点升高还是降低? 。
(3)某温度下,向1L密闭容器中开始充入2molSO2和1molO2,在V2O5催化剂存在时反应达到平衡,压强减小为开始时的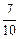 ;如在相同温度下,在同等体积的密闭容器中充入2mol的SO3,也在V2O5催化剂存在时反应达到平衡,求此温度下反应2SO3 (g)
;如在相同温度下,在同等体积的密闭容器中充入2mol的SO3,也在V2O5催化剂存在时反应达到平衡,求此温度下反应2SO3 (g)  2SO2(g) + O2(g)的平衡常数(写出计算过程)
2SO2(g) + O2(g)的平衡常数(写出计算过程)
(Ⅱ)化学试剂的生产和电镀工业排放的废水中常含有20~100mg.L-1Cr(Ⅵ),饮用含Cr(Ⅵ)的水会损害人的肠胃等,已知Cr(Ⅲ)的毒性是Cr(Ⅵ)的0.5%,国家规定工业废水含Cr(Ⅵ)的量排放标准为0.1mg.L-1。工业上常用化学法和电解法处理含Cr(Ⅵ)废水,再将Cr(Ⅲ)转化成沉淀除去,某研究性学习小组为研究废水的净化,设计了如下实验流程:
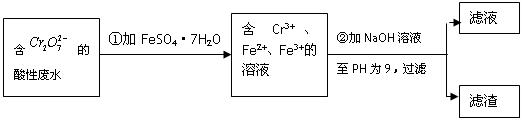
(1)配平第①步反应的离子方程式:
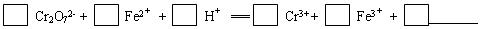
(2)第②步中用PH试纸测定溶液PH的操作是:
(3)设计一个电解装置也可以实现上述目的,装置如下图(用铁棒和石墨作电极):
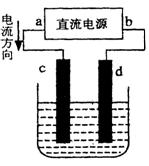
电极材料:c为:
电极反应:d极:
参考答案:
Ⅰ. (1)反应物总能量 (1分)
本题解析:略
本题难度:简单
4、选择题 单斜硫和正交硫转化为二氧化硫的能量变化如图所示,下列说法正确的是 ( )
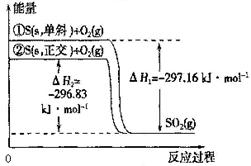
A.S(s,单斜) = S(s,正交) △H =" +" 0.33 kJ・mol-1
B.相同物质的量的正交硫比单斜硫所含有的能量高
C.正交硫比单斜硫稳定
D.①表示断裂1mol O2中的共价键所吸收的能量比形成l mol SO2中的共价键所放出的能量少297.16 kJ
参考答案:C
本题解析:
试题分析:A.根据图示可知单斜硫的能量比正交硫的能量高,所以S(s,单斜) = S(s,正交) △H = - 0.33 kJ/mol,错误;B.相同物质的量的正交硫比单斜硫所含有的能量低,错误;C.物质所含有的能量越低,物质的稳定性就越强,由于正交硫比单斜硫的能量低,所以正交硫比单斜硫稳定,正确;D.①表示断裂1mol O2中的共价键和单斜硫的化学键所吸收的能量比形成l mol SO2中的共价键所放出的能量少297.16 kJ,错误。
考点:考查物质的能量高低与稳定性及与化学键的键能的关系的知识。
本题难度:一般
5、填空题 A、B、C、D均为中学化学中常见的单质或化合物,它们之间的关系如图所示(部分产物已略去)
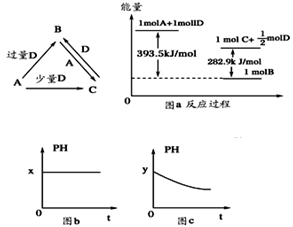
(1)若A为金属单质,D是某强酸的稀溶液,则反应C+D→B的离子方程式为_________
(2)若A、B为盐,D为强碱,A的水溶液显酸性,则 ①C的化学式为___________
②反应B+A→C的离子方程式为____________。
(3)若A为强碱,D为气态氧化物。常温时,将B的水溶液露置于空气中,其pH随时间t变化可能如上图的图b或图c所示(不考虑D的溶解和水的挥发)
①若图b符合事实,则D为________(填化学式),此时图b中x________7(填“
参考答案:
本题解析:
本题难度:困难