微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 当1g氨气完全分解为氮气、氢气时,吸收2.72kJ的热量,则下列热化学方程式正确的是( )
①N2(g)+3H2(g)═2NH3(g)△H=-92.4kJ/mol
②N2(g)+3H2(g)═2NH3(g)△H=-46.2kJ/mol
③NH3(g)═
1
2
N2(g)+3
2
H2(g)△H=+46.2kJ/mol
④2NH3(g)═N2(g)+3H2(g)△H=-92.4kJ/mol.
A.①②
B.①③
C.①②③
D.全部
2、选择题 热化学方程式C(s)+H2O(g) CO(g)+H2(g);△H=+131.3kJ/mol表示 CO(g)+H2(g);△H=+131.3kJ/mol表示
[???? ]
A.碳和水反应吸收131.3kJ能量
B.1mol碳和1mol水反应生成一氧化碳和氢气并吸收131.3kJ热量
C.1mol固态碳和1mol水蒸气反应生成一氧化碳气体和氢气,并吸热131.3kJ
D.1个固态碳原子和1分子水蒸气反应吸热131.1kJ
3、填空题 (16分)氮元素的化合物应用十分广泛。请回答:
(1)火箭燃料液态偏二甲肼(C2H8N2)是用液态N2O4作氧化剂,二者反应放出大量的热,生成无毒、无污染的气体和水。已知室温下,1 g燃料完全燃烧释放出的能量为42.5kJ,则该反应的热化学方程式为 。
(2)298 K时,在2L固定体积的密闭容器中,发生可逆反应:2NO2(g) N2O4(g)ΔH=-a kJ·mol-1 (a>0) 。N2O4的物质的量浓度随时间变化如图。达平衡时,N2O4的浓度为NO2的2倍,回答下列问题: N2O4(g)ΔH=-a kJ·mol-1 (a>0) 。N2O4的物质的量浓度随时间变化如图。达平衡时,N2O4的浓度为NO2的2倍,回答下列问题:
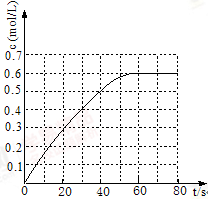
①298k时,该反应的平衡常数为 L ·mol-1(精确到0.01)。
②下列情况不是处于平衡状态的是 :
A.混合气体的密度保持不变; B.混合气体的颜色不再变化; C.气压恒定时。
③若反应在398K进行,某时刻测得n(NO2)="0.6" mol n(N2O4)=1.2mol,则此时V(正) V(逆)(填“>”、“<”或“=”)。
(3)NH4HSO4在分析试剂、医药、电子工业中用途广泛。现向100 mL 0.1 mol·L-1NH4HSO4溶液中滴加0.1 mol·L-1NaOH溶液,得到的溶液pH与NaOH溶液体积的关系曲线如图所示。

试分析图中a、b、c、d、e五个点,
①b点时,溶液中发生水解反应的离子是______;
②在c点,溶液中各离子浓度由大到小的排列顺序是 。
4、填空题 (1)实验测得,5g甲醇在氧气中充分燃烧生成二氧化碳气体和液态水时释放出113.5kJ的热量,试写出甲醇燃烧的热化学方程式: 。
(2)已知反应N2(g)+3H2(g) 2NH3(g) △H=a kJ/mol。试根据表中所列键能数据估算a的数值: 。 2NH3(g) △H=a kJ/mol。试根据表中所列键能数据估算a的数值: 。
化学键
| H—H
| N—H
| N=N
| 键能(kJ/mol)
| 436
| 391
| 945
(3)依据盖斯定律可以对某些难以通过实验直接测定的化学反应的焓变进行推算。
已知:
C(s,石墨)+O2(g) CO2(g) △H1=-393.5kJ?mol-1 ①
2H2(g)+O2(g) 2H2O(1) △H2=-571.6kJ?mol-1 ②
2C2H2(g)+5O2(g) 4CO2(g)+2H2O(l) △H3 =-2599kJ?mol-1 ③
根据盖斯定律,计算298K时由C(s,石墨)和H2(g)生成1mol C2H2(g)反应的焓变: 。
5、选择题 根据以下三个热化学方程式:
(1)2H2S(g)+3O2(g)=2SO2(g)+2H2O(l) ΔH= -Q1kJ·mol-1
(2)2H2S(g)+O2(g)=2S(g)+2H2O(g) ΔH= -Q2kJ·mol-1
(3)2H2S(g)+O2(g)=2S(g)+2H2O(l) ΔH= -Q3kJ·mol-1
判断 三者关系正确的是 三者关系正确的是
A.Q1>Q2>Q3
B.Q1>Q3>Q2
C.Q3>Q2>Q1
D.Q2>Q1>Q3
|
|
|
网站客服QQ: 960335752 - 14613519 - 791315772