��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1��ѡ����
����˵����ȷ����
[???? ]
A����Ϊ��������������Һ���Է�����Ӧ���ʲ���������������Һ��ȥ�����������Ĥ
B�������ƿ���ˮ��Ӧ���ʲ����ý������û���������
C��п�Ļ�Ա���ǿ�����ں������������п���Լ����ִ���ʴ
D��ͭ�̵���Ҫ�ɷ���������ͭ���������ȥͭ��
�ο��𰸣�C
���������
�����Ѷȣ���
2��ѡ���� þ���Ͻ���������ȫ��Ӧ�������������������Һ�����Ľ���ǣ�������
A��û�г���������
B��ֻ������������������
C��ֻ��������þ��������
D��������������������þ��������
�ο��𰸣�C
���������
�����Ѷȣ�һ��
3��ѡ���� ijNa2CO3��NaAlO2�Ļ����Һ����μ���1mol��L-1�����ᣬ�����Һ�е�CO32-��HCO3-��AlO2-��Al3+���ӵ����ʵ��������������Һ������仯��ϵ��ͼ��ʾ��������˵����ȷ����
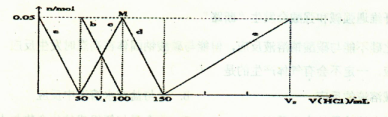
A��ԭ�����Һ�е�CO32-��AlO2-�����ʵ���֮��Ϊ1��2
B��V1��V2=1��5
C��M��ʱ���ɵ�CO2Ϊ0��05mol
D��a���߱�ʾ�����ӷ���ʽΪ��AlO2-+H++H2O=Al��OH��3��
�ο��𰸣�D
�����������
�����Ѷȣ�һ��
4��ѡ���� ��֪��Cu+2Fe3+�T2Fe2++Cu2+���ְ���ͬ���ʵ�����CuSO4��FeCl3��Zn����ˮ�г�ַ�Ӧ����Ӧ���û�����г�����SO42-��Cl-�⣬������
A.Zn2+��Cu��Fe3+
B.Zn��Cu2+��Fe3+
C.Zn2+��Cu2+��Fe2+
D.Zn2+��Cu��Cu2+��Fe2+
�ο��𰸣�D
������������������ݽ�����Է�Ӧ���Ⱥ�˳���ڽ������˳���У����ǿ�Ľ����ܽ�������Ľ�����������Һ���û����������ԣ�����Zn��FeCl3��Ӧ��������Zn��CuSO4��Ӧ���ݴ˼��ɽ��
��𣺰���ͬ���ʵ�����CuSO4��FeCl3��Zn����ˮ�г�ַ�Ӧ�������ǵ����ʵ�����Ϊ1mol�����ݷ�Ӧ˳���жϣ�
����? Zn+2FeCl3=ZnCl2+2FeCl2��Zn+CuSO4 =ZnSO4 +Cu
??? 0.5mol??? 1mol???????????????? 0.5mol???0.5mol????
ʣ��0.5molZn��ʣ��0.5molCuSO4������??0.5molCu��
��Ӧ���û�����г�����SO42-��Cl-�⣬������Zn2+��Cu��Cu2+��Fe2+��
��ѡ��D��
���������⿼���˽������˳���Ӧ�ã����ݽ������˳���������н���ǹؼ�����Ŀ�ϼ�
�����Ѷȣ�����
5��ѡ���� ����ʵ�����Ӧʾ��ͼ�Ĺ�ϵ��ȷ����????