微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 下列说法中,正确的是 [???? ]
A. 硅的化学性质不活泼,在自然界中可以以游离态存在
B. 工业上制备镁是用电解熔融的MgCl2来完成的
C. Na2O和Na2O2含有的化学键类型完全相同,都能与硫酸溶液反应
D. SO2通入新制氯水中,氯水褪色是因为SO2具有漂白性
参考答案:B
本题解析:
本题难度:简单
2、选择题 下列物质与氧气反应,生成氧化物的种类最少的是?(???)
A.Li
B.Na
C.K
D.Rb
参考答案:A
本题解析:本题主要挖掘课本知识点Li与氧气反应只有Li2O。
本题难度:简单
3、选择题 在空气中久置而不易变质的是
A.烧碱
B.硅酸钠溶液
C.纯碱
D.碱石灰
参考答案:C
本题解析:略
本题难度:简单
4、填空题 甲、乙两个实验小组分别进行“测定Na2CO3和NaCl混合物中Na2CO3含量”的实验。
(1)甲组:沉淀分析法:
把一定量的混合物溶解后加入过量CaCl2,然后将所得沉淀过滤、洗涤、烘干、称量。确定CaCl2溶液是否过量的方法是????????????????????????????????洗涤沉淀并判断沉淀是否洗净的操作是_______________________________________。
(2)乙组:气体分析法:
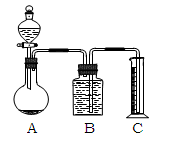
把一定量的混合物与足量盐酸反应后,用如图装置测定产生的CO2气体的体积,为减小CO2的溶解,B中溶液应是____________,选用该溶液后实验结果还是不准确,原因是_________________。
(3)请你设计一个与甲、乙两组操作不同的实验方案,测定混合
物中Na2CO3的含量。
方法:?????????????????????????????????????????????????????????????????;
试剂:_________________________________________________________________。
用到的玻璃仪器:_______________________________________________(至少2件)。
参考答案:(1)静置,向上层清液中继续滴加CaCl2溶液,若无沉淀说明
本题解析:
试题分析:(1)确定CaCl2溶液是否过量的方法是继续滴加沉淀剂,所以正确的操作是静置,向上层清液中继续滴加CaCl2溶液,若无沉淀说明CaCl2已过量;洗涤沉淀需要在过滤器中洗涤,即沿玻棒向过滤器中的沉淀上加蒸馏水至淹没沉淀,静置使其全部滤出,重复2~3次。由于洗涤液中含有氯离子,则判断沉淀是否洗净的操作是向滤液(洗涤液)中滴加AgNO3溶液判断是否洗净。
(2)要减少CO2的溶解,则应该用饱和的碳酸氢钠溶液。由于盐酸以挥发,则生成的CO2中含有氯化氢,而HCl会与NaHCO3反应生成CO
本题难度:一般
5、填空题 写出下列反应的离子方程式。
(1)过量CO2与KOH溶液反应:__________________________________________。
(2)足量NaOH溶液与Ca(HCO3)2溶液反应:_______________________________。
(3)苛性钾加入小苏打溶液中正好完全反应:_____________________________。
参考答案:(1)OH-+CO2==== 本题解析:(1)CO2不足时,生成碳酸盐;CO2过量时,生成酸式碳酸盐,即
本题解析:(1)CO2不足时,生成碳酸盐;CO2过量时,生成酸式碳酸盐,即
2NaOH+CO2(不足)====Na2CO3+H2O(继续通入CO2,反应仍能进行,可见CO2不过量);
NaOH+CO2====NaHCO3(继续通入CO2,不再发生反应,可见CO2已过量)
(2)NaOH与Ca(HCO3)2的反应,也有2种情况:NaOH不足时,Ca(HCO3)2部分被中和;NaOH过量时,Ca(HCO3)2完全被中和:
 本题难度:简单
本题难度:简单