微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、填空题 (本题共12分)
Ⅰ、氮元素的氢化物和氧化物在工业生产和国防建设中都有广泛应用。回答下列问题:
(1)氮元素原子的L层电子数为??????????;
(2) NH3与NaClO反应可得到肼(N2H4),该反应的化学方程式为???????????????????????????;
(3)肼可作为火箭发动机的燃料,与氧化剂N2O4反应生成N2和水蒸气。
已知:①N2(g)+2O2(g) = N2O4(l)???????? ΔH1=-19.5kJ?mol-1
②N2H4(l) + O2 (g)=N2(g)+2H2O(g)? ΔH2 ="-534.2" kJ・mol-1
写出肼和N2O4反应的热化学方程式?????????????????????????????????????;
(4)肼一空气燃料电池是一种碱性电池,该电池放电时,负极的反应式为?????????????。
Ⅱ、一定质量的液态化合物 在标准状况下的一定质量的
在标准状况下的一定质量的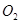 中恰好完全燃烧,反应方程式为:
中恰好完全燃烧,反应方程式为: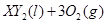 ===
=== 冷却后,在标准状况下测得生成物的体积是672 mL,密度是2.56
冷却后,在标准状况下测得生成物的体积是672 mL,密度是2.56 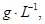 则:
则:
(1)反应前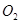 的体积是??????????。?? (2)化合物
的体积是??????????。?? (2)化合物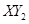 的摩尔质量是???????????。
的摩尔质量是???????????。
(3)若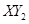 分子中X、Y两元素的质量比是3∶16,则X、Y两元素分别为???和????(写元素符号)。
分子中X、Y两元素的质量比是3∶16,则X、Y两元素分别为???和????(写元素符号)。
参考答案:I、(1)5?(2)2NH3+NaClO==N2H4+NaC
本题解析:I、 (1)N原子的原子结构示意图为: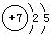 ,故其L层上有5个电子;
,故其L层上有5个电子;
(2)NH3+NaClO――N2H4,根据元素守恒还应生成NaCl和H2O,观察法可配平方程式为 2NH3+NaClO==N2H4+NaCl+H2O;
(3)肼与N2O4反应生成N2和水蒸气:2N2H4 +N2O4==3N2+4H2O,
本题难度:一般
2、选择题 某金属的硝酸盐加热分解生成的NO2和O2的物质的量之比为8∶1。在加热过程中,该金属元素的化合价(???)
A.降低
B.升高
C.不变
D.无法确定
参考答案:B
本题解析: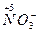 ―
―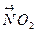 ?
? 本题难度:简单
本题难度:简单
3、选择题 下列关于硝酸的说法中正确的是?(??)
A.稀硝酸能与Fe发生反应,浓硝酸不能
B.浓硝酸和稀硝酸都是强氧化剂
C.稀硝酸是弱酸,浓硝酸是强酸
D.稀硝酸与Cu反应生成NO,而浓硝酸与Cu反应生成NO2,稀硝酸得电子更多,故稀硝酸的氧化性大于浓硝酸
参考答案:B
本题解析:
试题分析:浓硝酸和铁也反应,A不正确;硝酸都是强酸,C不正确;D不正确,浓硝酸的氧化性强于稀硝酸的,这与得到电子的多少无关系,只与得到电子的难易程度有关系,答案选B。
点评:该题是高考中的常见题型和考点,属于基础性试题的考查,难度不大。主要是有利于巩固学生的基础知识,提高学生灵活运用基础知识解决实际问题的能力。该题的关键是要注意氧化性或还原性强弱,只与得失电子的难易程度有关系,而与得失电子的得失无关,需要灵活运用。
本题难度:简单
4、选择题 将充满20mLNO的试管倒置于盛有蒸镏水的烧杯中,然后向试管里通入纯氧气,当试管内液面稳定在试管容积的4/5时,则通入O2为
①12 mL??②3 mL??③19 mL??④31 mL
A.①④
B.①③
C.②③
D.③④
参考答案:B
本题解析:本题发生的反应可用下式表示:4NO+3O2+2H2O=4HNO3,最后剩余气体20/5=4mL,为O2或NO,设当NO过量时,通入O2为a,
4NO+3O2+2H2O=4HNO3
4??? 3
20-4 a?? a=12mL
?设当O2过量时,通入O2为b,
4NO+3O2+2H2O=4HNO3
4??? 3
20?? b-4??? b=19mL,则 B正确。
本题难度:一般
5、选择题 下列物质中,分别加入少量溴水,振荡后静置,水溶液呈无色的是
A.NaOH溶液
B.NaCl溶液
C.KI溶液
D.四氯化碳
参考答案:AD
本题解析:
试题分析:A、Br2与NaOH溶液反应,生成NaBrO、NaBr和水,故溴水褪色,正确;B、溴水与NaCl溶液混合时不反应,故不褪色,错误;C、Br2与KI反应,生成KBr和I2,溶液的颜色加深,错误;D、四氯化碳从水中溶解、分离出I2,液体分层后,水层褪色,正确。
本题难度:一般