微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 浓硝酸与下列物质反应时,既表现氧化性,又表现酸性的是(???)
A.Cu(OH)2
B.Cu
C.木炭
D.FeO
参考答案:BD
本题解析:浓HNO3在反应过程中得电子表现出氧化性,若有盐生成,则表现出酸性。
本题难度:简单
2、选择题 如图所示,在干燥的圆底烧瓶中充满某气体a,胶头滴管中吸有少量液体b,当把溶液b挤进烧瓶后,打开止水夹不能形成“喷泉”的组合是
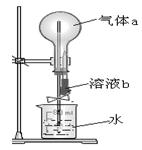
?
| 干燥气体a
| 液体b
|
A
| NH3
| 水
|
B
| HCl
| 水
|
C
| CO2
| NaOH溶液
|
D
| Cl2
| 饱和食盐水
参考答案:D
本题解析:略
本题难度:一般
3、填空题 NOx是汽车尾气中的主要污染物之一。
(1)NOx能形成酸雨,写出NO2转化为HNO3的化学方程式:_________________________________________________________。
(2)汽车发动机工作时会引发N2和O2反应,其能量变化示意图如下:
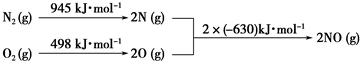
①写出该反应的热化学方程式:_______________________________________。
②随温度升高,该反应化学平衡常数的变化趋势是____。
(3)在汽车尾气系统中装置催化转化器,可有效降低NOx的排放。
①当尾气中空气不足时,NOx在催化转化器中被还原成N2排出。写出NO被CO还原的化学方程式:____________________________________。
②当尾气中空气过量时,催化转化器中的金属氧化物吸收NOx生成盐。其吸收能力顺序如下:12MgO<20CaO<38SrO<56BaO。原因是_____________________________________________,
元素的金属性逐渐增强,金属氧化物对NOx的吸收能力逐渐增强。
(4)通过NOx传感器可监测NOx的含量,其工作原理示意图如下:
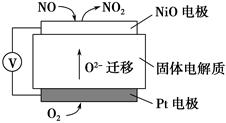
①Pt电极上发生的是________反应(填“氧化”或“还原”)
②写出NiO电极的电极反应式:_______________________________________。
参考答案:(1)3NO2+H2O=2HNO3+NO
(2)①N2
本题解析:(1)NO2转化为HNO3的化学方程式为:3NO2+H2O=2HNO3+NO。
(2)①拆开化学键吸收能量,形成化学键释放能量
N2(g)+O2(g)=2NO(g)其ΔH计算方法如下
ΔH=945 kJ・mol-1+498 kJ・mol-1-2×630 kJ・mol-1=+183 kJ・mol-1
②该反应为吸热反应,升高温度,化学平衡向正反应方向移动,化学平衡常数增大。
(3)①NO和CO发生反应生成N2和CO2,其化学方程式为2CO+2NO 本题难度:一般 本题难度:一般
4、实验题 (13分)现给你一试管二氧化氮,其他药品和仪器自选。试设计实验,要求尽可能多地使二氧化氮被水吸收。
?
| 实验步骤
| 现象
| 解释(可用化学方程式表示)
| (1)
| ?
| ?
| ?
| (2)
| ?
| ?
| ?
| (3)
| ?
| ?
| ?
?
参考答案:
?
实验步骤
现象
解释(可用化学
本题解析:根据3NO2+H2O====2HNO3+NO及2NO+O2====2NO2可知,4NO2+O2+2H2O====
4HNO3,即可补充氧气使二氧化氮能尽可能多地溶于水。
本题难度:简单
5、填空题 [化学―选修化学与技术](15分)
工业上常用 氨氧化法生产硝酸,其生产过程包括氨的催化氧化(催化剂为铂铑合金丝网)、一氧化氮的氧化和水吸收二氧化氮生成硝酸。请回答下列问题:
⑴氨催化氧化反应在一定温度下(水为气体)为正反应放热的可逆反应,写出该反应的化学方程式????????????????????????????????和平衡常数表达式K=???????????????,若升高温度,则K的值??????(填“增大”“减小”或“不变”)。
⑵为了提高NH3的转化率,可以采取???????。
a.减小压强b.增大反应物浓度c.使用催化剂d.降低温度e.及时分离出NH3
⑶原料气中空气必须过量,其主要原因是?????????????????????????????????????????。
⑷将铂铑合金做成薄丝网的主要原因是???????????????????????????????????????????。
⑸水吸收二氧化氮生成硝酸为放热反应,其化学方程式为????????????????????????????,
为了提高水对二氧化氮的吸收率,可采取的措施为??????????????????????????????(答2项)。
参考答案:
 本题解析:(1)在书写化学平衡常数的时候,注意水不要漏掉;(2)根据该反应的正反应是吸热反应,可以采用降低温度的方法,该反应的正反应是体积增大的反应,可以采用减小压强的方法,增大反应物的浓度,反应向正方向进行,故选abd;(3)空气过量,即增大了氧气的浓度,反应朝有利于NO生成的方向进行;(4)做成网状主要是增大单位质量的催化剂与反应物的接触面积;(5)方程式是3NO2+H2O=2HNO3+NO,提高水对二氧化氮的吸收率,就是提高NO2的转化率,可以采用加压、降温的方法。 本题解析:(1)在书写化学平衡常数的时候,注意水不要漏掉;(2)根据该反应的正反应是吸热反应,可以采用降低温度的方法,该反应的正反应是体积增大的反应,可以采用减小压强的方法,增大反应物的浓度,反应向正方向进行,故选abd;(3)空气过量,即增大了氧气的浓度,反应朝有利于NO生成的方向进行;(4)做成网状主要是增大单位质量的催化剂与反应物的接触面积;(5)方程式是3NO2+H2O=2HNO3+NO,提高水对二氧化氮的吸收率,就是提高NO2的转化率,可以采用加压、降温的方法。
本题难度:一般
|
|