微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 短周期元素X、Y、Z、M、R在周期表中的相对位置如图所示。下列说法正确的是
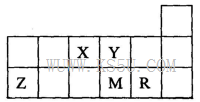
A.元素X和M的氧化物对应的水化物均为强酸
B.R的单质能与M的氢化物发生置换反应
C.气态氢化物的稳定性:M>Y
D.元素Y、Z形成的简单离子半径大小关系为:Z>Y
参考答案:B
本题解析:
本题难度:简单
2、选择题 根据元素周期表和元素周期律,判断下列有关描述正确的是(??)
A.碱金属元素中,金属活泼性最强的是Li
B.第三周期元素中,原子半径最大的是Cl
C.短周期元素最高价氧化物对应的水化物中,酸性最强的是H2SO4
D.原子序数为11与9的元素能够形成离子化合物,该化合物中存在离子键
参考答案:D
本题解析:
本题难度:一般
3、选择题 下列各组顺序的排列不正确的是
A.离子半径:Na+>Mg2+>Al3+>F―
B.热稳定性:HCl>H2S>PH3
C.酸性强弱:Al(OH)3<H2SiO3<H2CO3<H3PO4
D.熔点:SiO2>NaCl>Na>CO2
参考答案:A
本题解析:
本题难度:一般
4、填空题 (14分)现有前20号的A、B、C、D、E五种元素,相关信息于下表:
元素
| 信息
|
A
| 元素的核外电子数和电子层数相等,也是宇宙中最丰富的元素
|
B
| B原子得一个电子后2p轨道全满
|
C
| C原子的p轨道中有3个未成对电子,其气态氢化物在水中的溶解度在同族元素所形成的氢化物中最大
|
D
| D的最高化合价和最低化合价的代数和为4,其最高价氧化物中含D的质量分数为40%,且其核内质子数等于其中子数
|
E
| E+和B- 具有相同的电子层结构 具有相同的电子层结构
(1)B的核外电子排布式为________?,CB3的晶体类型为________ 。
(2)B、C、D三元素的电负性大小顺序为________>________>________(填元素符号)。
(3)C的氢化物的空间构型为________,其氢化物在同族元素所形成的氢化物中沸点最高的原因是______________________________________________________。
(4)E2D的水溶液呈?????(填“酸性”、“碱性”或“中性”),用离子方程式解释理由:_______________________。
(5)已知:12.8 g液态C2 A4与足量A2O2反应生成C2和气态A2O,放出256.65 kJ的热量。
A2O (l)=== A2O (g) ΔH=+44 kJ・mol-1。
2 A2O2 (l)===2A2O (l)+O2(g) ΔH=-196.4 kJ・mol-1。
则液态C2 A4与足量O2反应生成C2和液态A2O的热化学方程式为:??? ________________________________________________。
参考答案:(1)1s22s22p5?(2分)分子晶体(1分)?
本题解析:
本题难度:一般
5、填空题 (10分)五种元素A、B、C、D、E位于元素周期表的前四周期,已知它们的核电荷数依次增加,A是宇宙中含量最多的元素;B原子的L层p轨道中有2个电子;C与B原子的价层电子数相同;D原子M层的d轨道有一个成对电子;E原子的L层电子数与最外层电子数之比为4:1,其d轨道中的电子数与最外层电子数之比为5:1。
(1)B与A形成只含一个中心原子的共价化合物,其分子的电子式为????????,中心原子的杂化轨道类型是 ????????,其分子的的立体构型是?????????
(2)A的氧化物与B的氧化物中,分子极性较小的是(填分子式)__________
(3)B与C比较,电负性较大的(填元素名称)____________
(4)写出D的价层电子排布式??????????????????????????
(5)E与Al的化学性质相似,请写出E与NaOH溶液反应的化学方程式????????????????????????
(6)写出D的最高价氧化物与盐酸反应的离子方程式????????????????????????????
参考答案:(10分)(1)电子式?????????????
本题解析:
本题难度:简单
|