微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、计算题 硫酸的工业制备是一个重要的化工生产过程,但同时在生产过程中会产生大量SO2等污染物。
(1)将SO2通入Fe(NO3)3溶液中,溶液由棕黄色变为浅绿色,但立即又变为棕黄色,此时若滴入BaCl2溶液,则会产生白色沉淀。溶液由棕黄色变为浅绿色用离子方程式表示为_____,后又由浅绿色变为棕黄色的离子方程式为_____。
(2)以硫酸工业的尾气、氨水、石灰石、焦炭及碳酸氢铵和KCI为原料可以合成有重要用途的硫化钙、硫酸钾、亚硫酸氢铵等物质。合成路线如下:
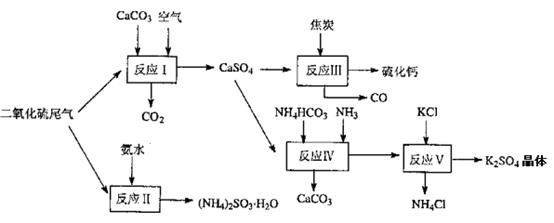
写出反应反应Ⅳ的化学方程式????????????????????;
反应III中氧化剂与还原剂的物质的量之比为__?????????__;
反应V在25"C、40%乙二醇溶液中进行,该复分解反应能顺利进行的原因是?????????。
(3)新型纳米材料氧缺位铁酸锌(ZnFe2Ox),常温下能使SO2分解,减小工业废气对环境的影响,它由铁酸锌(ZnFe2O4)经高温还原制得,转化流程如下图所示:
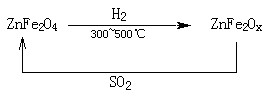
若2molZnFe2Ox与SO2反应可生成 0.75molS,x=??????,写出铁酸锌高温下被还原生成氧缺位铁酸锌的化学方程式???????????????????
(4)石灰石-石膏湿法烟气脱硫工艺技术的原理是烟气中的二氧化硫与浆液中的碳酸钙以及空气反应生成石膏(CaSO4.2H2O),写出该反应的化学方程式?????????。某电厂用煤300t(煤中含硫的质量分数为2.5%),若燃烧时煤中的硫全部转化为二氧化硫,用该方法脱硫时有96%的硫转化为石膏,则可生产石膏?????????t。
参考答案:(共16分)(1)SO2 + 2Fe3+ + 2H2O=SO
本题解析:
试题分析:(1)SO2具有还原性,铁离子具有氧化性,铁离子能把SO2氧化生成硫酸,而铁离子被还原为亚铁离子,所以溶液由棕黄色变为浅绿色,反应的离子方程式是SO2 + 2Fe3+ + 2H2O=SO42- + 2Fe2+ + 4H+。由于在酸性条件下,NO3-具有强氧化性,能把亚铁离子氧化生成铁离子,因此又由浅绿色变为棕黄色,反应的离子方程式为3Fe2+ + NO3- + 4H+=3Fe3+ + NO↑+ 2H2O。
(2)反应Ⅳ的反应物有硫酸钙、碳酸氢铵和氨气,生成物之一是碳酸钙,则根据原子
本题难度:一般
2、选择题 化学与生产、生活、科技等密切相关.下列说法正确的是( )
A.煤经气化和液化两个物理变化过程,可变为清洁能源
B.国务院要求坚决控制钢铁、水泥、焦炭等行业产能总量是落实“低碳经济”的具体举措
C.绿色化学的核心是应用化学原理对环境污染进行治理
D.“神州七号”的防护层中含聚四氟乙烯,聚四氟乙烯属于不饱和烃
参考答案:B
本题解析:
本题难度:简单
3、填空题 硫铁矿烧渣是硫铁矿生产硫酸过程中产生的工业废渣(主要含Fe2O3及少量SiO2、Al2O3、CaO、MgO等杂质)。用该烧渣制取药用辅料――红氧化铁的工艺流程如下:
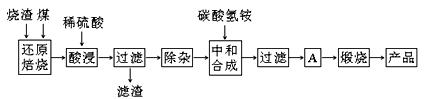
(1)在“还原焙烧”中产生的有毒气体可能有???????????????。
(2)“酸浸”时间一般不超过20 min,若在空气中酸浸时间过长,溶液中Fe2+含量将下降,其原因用离子方程式表示:?????????????????????????????。
(3)根据下表数据:
氢氧化物
| Al(OH)3
| Mg(OH)2
| Fe(OH)3
| Fe(OH)2
|
开始沉淀的pH
| 3.10
| 8.54
| 2.01
| 7.11
|
完全沉淀的pH
| 4.77
| 11.04
| 3.68
| 9.61
在“除杂”步骤中,为除去Fe3+和Al3+,溶液的pH最大值应小于??,当pH=5时,溶液中c(Al3+)为?????mol・L-1(已知常温下Ksp[Al(OH)3]=2.0×10-33)。
(4)“中和合成”的目的是将溶液中Fe2+转变为碳酸亚铁沉淀,碳酸氢铵与硫酸亚铁反应的离子方程式为?????????????????????????????????????????????。
若用等物质的量的碳酸铵替代碳酸氢铵,则产品中可能混有的杂质是???????。
(5)A的操作是????????????????????。
(6)m g烧渣经过上述工艺可得红氧化铁n g。药典标准规定,制得的红氧化铁中含氧化铁不得少于98.0%,则所选用的烧渣中铁的质量分数应不低于???????????(用含m、n的表达式表示)。
参考答案:(1)CO和SO2等(写出一个合理答案也给分) ??????
本题解析:略
本题难度:简单
4、选择题 “绿色化学”是当今社会提出的一个新概念.在“绿色化学工艺中,理想状态是反应中原子全部转化为欲制的产物,即原子利用率为100%。以下反应最符合绿色化学概念的是
[???? ]
A.乙烯聚合为聚乙烯高分子材料
B.甲烷与氯气制备一氯甲烷
C.以铜和浓硝酸为原料生产硝酸铜
D.用二氧化硅制备高纯硅
参考答案:A
本题解析:
本题难度:简单
5、选择题 工业生产中物质制备时,通过下列的反应原理一步完成获得产物,符合“绿色化学”原则的反应原理是[???? ]
A.加成反应
B.分解反应
C.取代反应
D.置换反应
参考答案:A
本题解析:
本题难度:简单
|