微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 NH4Cl溶液中,下列叙述正确的是
A.c(NH4+)>c(Cl-) >c(OH-) >c( H+ )
B.c(Cl-)>c(NH4+)>c( H+ )>c(OH-)
C.c(NH4+) + c( NH3) = c(Cl-) + c(OH-)
D.c(NH4+) + c( NH3 ・ H2O) + c( NH3 )= c(Cl-)
参考答案:BD
本题解析:氯化铵由于NH4+水解,溶液显酸性,A不正确,B正确。根据电荷守恒c(NH4+) + c(H+) = c(Cl-) + c(OH-)可知C是错误的。根据氮原子守恒可知,D正确。答案选BD。
本题难度:困难
2、选择题 要除去MgCl2酸性溶液中少量的FeCl3,不宜选用的试剂是
A.MgO
B.MgCO3
C.NaOH
D.Mg(OH)2
参考答案:C
本题解析:
试题分析:在解答物质分离提纯试题时,选择试剂和实验操作方法应遵循三个原则: 1.不能引入新的杂质(水除外),即分离提纯后的物质应是纯净物(或纯净的溶液),不能有其他物质混入其中;2.分离提纯后的物质状态不变;3.实验过程和操作方法简单易行,即选择分离提纯方法应遵循先物理后化学,先简单后复杂的原则,据此可以判断。A、氧化镁能消耗溶液中的氢离子,降低溶液的酸性,进而可以生成氢氧化铁沉淀,且不会引入新的杂质,A正确;B、碳酸镁能消耗溶液中的氢离子,降低溶液的酸性,进而可以生成氢氧化铁沉淀,且不会引入新的杂质,B正确;C、氢氧化钠能消耗溶液中的氢离子,使铁离子转化为氢氧化铁沉淀。但同时又引入了新的杂质钠离子,C不正确;D、氢氧化镁能消耗溶液中的氢离子,降低溶液的酸性,进而可以生成氢氧化铁沉淀,且不会引入新的杂质,D正确,答案选C。
考点:考查物质除杂的有关判断
本题难度:一般
3、填空题 常温下有0. 1 mol/L的以下几种溶液,①H2SO4溶液②NaHSO4溶液③CH3COOH溶液④HCl溶液⑤HCN溶液⑥NH3・H2O,其中如下几种溶液的电离度(即已经电离的占原来总的百分数)如下表(已知H2SO4的第一步电离是完全的),回答下面问题:
①H2SO4溶液HSO4-
| ②NaHSO4溶液HSO4-
| ③CH3COOH
| ④HCl溶液
|
10%
| 29%
| 1.33%
| 100%
(1)常温下,pH相同的表格中几种溶液,其物质的量浓度由大到小的顺序是(填序号,下同) _
(2)常温下,将足量的锌粉投人等体积pH=1的表格中几种溶液中,产生H2的体积(同温
同压下)由大到小的顺序是_ _
(3)在25℃时,若用已知浓度的NaOH滴定未知浓度的CH3 COOH应选用_ 作指示剂,若终点时溶液pH = a,则由水电离的。c(H+)为_ 。
(4)在25℃时,将b mol・L-1的KCN溶液与0. O1 mol・L-1的盐酸等体积混合,反应达到平衡时,测得溶液pH = 7,则KCN溶液的物质的量浓度b_ 0.01 mol・L-1填“>”、“<”或“=”);用含b的代数式表示HCN的电离常数Ka=
参考答案:(1)③>②>④>①⑵③>②>
本题解析:
试题分析:(1)由于pH相同的几种溶液,即氢离子浓度相同,弱酸是难电离的,故③CH3COOH的浓度是最大,①H2SO4溶液HSO4-中可以看作是比一元强酸稍大的酸,故浓度最小。其物质的量浓度由大到小的顺序是③>②>④>①。 (2)常温下,将足量的锌粉说明酸完全反应了,这与酸最终提供的氢离子量有关,故顺序为③>②>①>④。 (3)由于终点时生成强碱弱酸盐呈碱性,因此选择在碱性范围内变色的指示剂,应选用酚酞作指示剂,若终点时溶液pH = a,此时OH-全是水电离产生,则由水电离的氢离子和氢氧根相等。c(H+)=10-(14-a)mol/L。(4)KCN+HCl
本题难度:困难
4、填空题 (10分)(1)AgNO3的水溶液呈 (填“酸”、“中”、“碱”)性,原因是(用离子方程式表示): ;
(2)氯化铝水溶液呈 性,(填“酸”、“中”、“碱”)性,原因是(用离子方程式表
示): ;
把AlCl3溶液蒸干,灼烧,最后得到的主要固体产物是 。
(3)已知MgCl2・6H2O晶体在空气中加热时,释放部分结晶水,同时生成Mg(OH)Cl(碱式氯化镁)或生成MgO。下列是关于MgCl2・6H2O的综合应用:
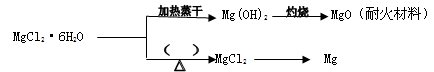
请回答下列问题:
①在上图的括号内应填的是在_______________环境中加热。
②Mg(OH)2固体存在如下溶解平衡:Mg(OH)2(固)  Mg2++2OH-。向体系中加入(请填出两种不同类别的物质)_____________________________________________________ 有利于Mg(OH)2溶解。 Mg2++2OH-。向体系中加入(请填出两种不同类别的物质)_____________________________________________________ 有利于Mg(OH)2溶解。
③已知AnBm的离子积=c (Am+) n ・c (Bn-) m,式中c (Am+) n和c (Bn-) m表示离子的物质的量浓度,在室温时若测得Mg(OH)2饱和溶液的pH值为11,其离子积为___________________。
参考答案:(1)酸, Ag++ H2O  本题解析:(1)AgNO3是强酸弱碱盐,水解显酸性。 本题解析:(1)AgNO3是强酸弱碱盐,水解显酸性。
(2)氯化铝也是强酸弱碱盐,水解显酸性。铝离子水解生成氢氧化铝和氯化氢,水解吸热,加热促进水解。同时氯化氢的挥发,进一步促进水解,所以最终得到的是氢氧化铝,灼烧得到氧化铝。
(3)氯化镁水解显酸性,所以要得到氯化镁晶体,在加热时需要防止水解,因此在硫化氢的气流中加热即可。根据氢氧化镁的溶解平衡可知,要促进溶解,就必须使平衡向正反应方向移动。所以可以通过消耗OH-或镁离子来实现。根据离子积常数的概念可知,离子积常数是电离出的离子的浓度的幂之积,Mg(OH)2饱和溶液的pH值为11,则OH-的浓度为10-3mol/L,则镁离子浓度为5×10-4mol/L,所以氢氧化镁的离子积常数为 。 。
本题难度:困难
5、选择题 关于小苏打水溶液的表述正确的是
A.c(Na+) = c(HCO3-) + c(CO32-) + c(H2CO3)
B.c(Na+)+ c(H+) = c(HCO3-) + c(OH-) + c(CO32-)
C.HCO3-的电离程度大于HCO3-水解程度
D.存在的电离有NaHCO3 = Na+ + HCO3-、HCO3-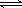 CO32-+ H+、H2O CO32-+ H+、H2O 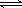 H+ + OH- H+ + OH-
参考答案:AD
本题解析:
试题分析:c(Na+) = c(HCO3-) + c(CO32-) + c(H2CO3),符合物料守恒,故A正确;根据电荷守恒,c(Na+)+ c(H+) = c(HCO3-) + c(OH-) +2 c(CO32-),故B错误;碳酸氢钠溶液呈碱性,HCO3-的电离程度小于HCO3-水解程度,故C错误;存在的电离有NaHCO3、HCO3-、H2O,故D正确。
考点:本题考查三大守恒。
本题难度:一般
|