微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 下列化学用语使用正确的是(???)
A.NH4Br的电子式:
B.S2-的结构示意图: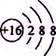
C.乙酸的分子式: CH3COOH
D.原子核内有l8个中子的氯离子: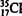
参考答案:B
本题解析:
试题分析:A项:氯化铵是离子化合物,由铵根离子与氯离子构成,其电子式为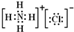 ,故错;C项:CH3COOH是结构简式,分子式应为:C2H6O,故错;D项:少些了离子的电荷符号应为:
,故错;C项:CH3COOH是结构简式,分子式应为:C2H6O,故错;D项:少些了离子的电荷符号应为: 本题难度:一般
本题难度:一般
2、选择题 下列氧化还原反应中,水作为氧化剂的是(?????)
A.CO + H2O CO2 + H2
CO2 + H2
B.3NO2+ H2O = 2HNO3 + NO
C.2Na2O2 + 2H2O =" 4NaOH" + O2↑
D.2F2 + 2H2O =" 4HF" + O2
参考答案:A
本题解析:
试题分析:A、H2O是氧化剂,正确;B、水既不是氧化剂,也不是还原剂,错误;C、H2O既不是氧化剂,也不是还原剂,错误; D、H2O是还原剂,错误。
本题难度:一般
3、选择题 (1)在一定温度和压强下,1体积X2(g)和3体积Y2(g)化合生成2体积Z(g),则Z气体的化学式是???????。
(2)A、B两种气体组成的混合气体8.6 g,在标准状况下体积为8.96 L。已知A与B的物质的量之比为3∶1,相对分子质量之比为14∶1,由此可推断A可能是?????????????????????????????????????????????,B可能是?????????。
(3)在标准状况下,CO和CO2的混合气体质量为36 g,体积为22.4 L,则CO所占的体积是?????L,质量是????????g。
参考答案:(1)XY3 (2)N2(或CO或C2H4) H2 (3)1
本题解析:(1)根据阿伏加德罗定律可写出化学方程式:X2+3Y2=2Z,再根据质量守恒定律,可得Z的化学式应为XY3。
(2)由题意可得:n(A)+n(B)=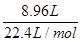 =0.4 mol,则3n(B)+n(B)=0.4 mol,即n(B)=0.1 mol,n(A)=0.3 mol。
=0.4 mol,则3n(B)+n(B)=0.4 mol,即n(B)=0.1 mol,n(A)=0.3 mol。
设B的相对分子质量为Mr,则A的相对分
本题难度:一般
4、填空题 有X、Y、Z三种元素,已知:
①X2-、Y-均与Y的气态氢化物分子具有相同的电子数;
②Z与Y可组成化合物ZY3,ZY3溶液遇KSCN溶液呈红色。
请回答下列问题:
(1)Y的最高价氧化物对应水化物的化学式是__________。
(2)将ZY3溶液滴入沸水可得到红褐色液体,反应的离子方程式是____________________。
此液体具有的性质是__________(填字母)。
a.光束通过该液体时形成光亮的“通路”
b.插入电极通直流电后,有一极附近液体颜色加深
c.向该液体中加入硝酸银溶液,无沉淀产生
d.将该液体加热、蒸干、灼烧后,有氧化物生成
(3)X单质在空气中燃烧生成一种无色有刺激性气味的气体。
①已知一定条件下,每1mol该气体被O2氧化放热98.0kJ。若2mol该气体与1mol O2在此条件下发生反应,达到平衡时放出的热量是176.4kJ,则该气体的转化率为__________。
②原无色有刺激性气味的气体与含1.5mol Y的一种含氧酸(该酸的某盐常用于实验室制取氧气)的溶液在一定条件下反应.可生成一种强酸和一种氧化物。若有1.5×6.02×1023个电子转移时,该反应的化学方程式是________________________________。
参考答案:(1)HClO4
(2)Fe3++3H2O![]()
本题解析:本题为元素推断题,属于经典题型。
(1)由ZY3遇KSCN溶液呈红色可知ZY3为FeCl3即Y为氯元素,由X2-、Y-与HCl具有相同的电子数(18个)可知X为硫元素;
(2)FeCl3滴入沸水中生成Fe(OH)3胶体,能发生丁达尔现象、电泳等;
(3)①S在空气中燃烧生成SO2,与O2进一步氧化:2SO2+O2 本题难度:一般
本题难度:一般
5、填空题 实验室可以用KMnO4固体和浓盐酸反应制取氯气,反应方程式如下:
2KMnO4+16HCl(浓)=2KCl+2MnCl2+5Cl2↑+8H2O。
①请用“双线桥”标出电子转移的方向和数目;(2分)
②该反应中被氧化和未被氧化的HCl的物质的量之比是 _______。(1分)
参考答案:① 本题解析:
本题解析:
试题分析:根据方程式2KMnO4+16HCl(浓)=2KCl+2MnCl2+5Cl2↑+8H2O可知,高锰酸钾中Mn元素的化合价从+7价降低到+2价,得到5个电子,高锰酸钾是氧化剂。氯化氢中氯元素的化合价从-1价升高到0价失去1个电子,氯化氢是还原剂。根据电子得失守恒可知,氧化剂与还原剂的物质的量之比1:5,据此可以用双线桥标出电子转移的方向和数目(见答案);根据方程式可知2mol高锰酸钾与16mol氯化氢反应,其中被氧化的氯化氢是5mol×2=10mol,则未被氧化的氯化氢是16mol-10mo
本题难度:简单