��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1��ѡ���� 11.2 g Cu��ijŨ��������ȫ�ܽ⣬��Ӧ����NO2��NO�������3.36L(��״��)������������NO2��NO�������Ϊ
A��1��l
B��1��2
C��1��3
D��2��l
�ο��𰸣�B
���������
���������11.2gͭ�����ʵ�����11.2g��64g/mol��0.175mol����״����3.36L�����������ʵ�����3.36L��22.4L/mol��0.15mol������������NO2��NO�����ʵ����ֱ���xmol��ymol������ԭ���غ�͵��ӵ�ʧ�غ��֪x+y��0.15��x+3y��0.175��2�����x��0.05��y��0.1�����Ի��������NO2��NO�������Ϊ1:2����ѡB��
���㣺������������ᷴӦ���йؼ���
�����Ѷȣ�һ��
2��ѡ���� �����йػ�ѧ����ı�����ȷ����
A����ȩ�ĵ���ʽ��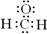
B��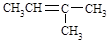 �����ƣ�3�D���D2�D��ϩ
�����ƣ�3�D���D2�D��ϩ
C����78�����ӵĵ�ķ����Ժ��أ�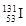
D��������Һ�ʼ��Ե�ԭ����CO32����2H2O��H2CO3��2OH��
�ο��𰸣�C
���������A����,����ʽ��̼ԭ�Ӻ���ԭ��֮����˫���ṹ.
B����,����Ӧ����2�D���D2�D��ϩ
C��ȷ.
D����,ˮ�ⷽ��ʽ��ȷӦ����CO32����H2O��HCO3-��OH-
�����Ѷȣ�һ��
3��ѡ���� �������ƣ�Na2FeO4�����Զ�����ˮ���о����������������з����Ƶã�
Fe2O3+3Na2O2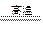 2Na2FeO4+Na2O��
2Na2FeO4+Na2O��
���ڸ÷�Ӧ˵����ȷ����
A��Na2FeO4���ڹ��ۻ�����
B����Ӧ��Na2O2��������
C������1 mol Na2FeO4����6 mol ����ת��
D����Na2FeO4��FeΪ+4�ۣ�����ǿ�����ԣ�������ɱ��
�ο��𰸣�B
�����������
�����Ѷȣ�һ��
4��ѡ���� �ڷ�Ӧ11P+15CuSO4+24H2O=5Cu3P+6H3PO4+15H2SO4�У�ÿĦ��CuSO4������P�����ʵ���Ϊ�� ��
A��1/5 mol
B��2/5 mol
C��3/5mol
D��11/5 mol
�ο��𰸣�A
���������
�������������ѡB��ӻ�ѧ����ʽ���Կ�����15molCuSO4����6molH3PO4������1mol CuSO4���� 2/5mol H3PO4����ԭ��û��ע��������е�H3PO4��һ����P����������ԭ��Ӧ���绯��Ӧ�����ɵġ�
�����⡿��ר�⸴ϰһ��Ҫ���۸����˳��ϵ����ȷ����Ԫ�ػ��ϼۼ���仯������ص�����1������ת�ƣ�2�������ԡ���ԭ�Լ���ǿ���жϣ�3����ؼ���ķ��������ɵȷ�������⡣�����еĻ�ԭ����P������������P��CuSO4�����ڷ�Ӧ������Cu��+2��Ϊ+1����˷�Ӧ�й��õ�15mol�ĵ��ӣ�������ԭ����P�ڷ�Ӧ�д�0����+5�ۣ����1mol P�õ�5mol���ӡ����15molCuSO4�ڷ�Ӧ������3mol��P����ÿĦ������ͭ�ܹ�����0.2mol��P
�����Ѷȣ�һ��
5������� Һ̬��������һ������������ǡ����ȫȼ�գ���Ӧ����ʽΪ��XY2��l��+3O2��g��=XO2��g��+2YO2��g����ȴ���ڱ�״���²��������������672ml���ܶ���2.56g/L��
��1����ӦǰO2�����Ϊ______��
��2��������XY2��Ħ��������______��
��3����XY2�����У�X��Y��Ԫ�ص�����֮��Ϊ3��16����X��Y��Ԫ�طֱ�Ϊ______��______��дԪ�����ƣ���
�ο��𰸣������������ʵ���Ϊn��XO2��+n��YO2��=
���������
�����Ѷȣ�һ��