微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、填空题 (10分)某地区用含较多Ca2+,Mg2+的天然水按照下列步骤制取蒸馏水。请回答下列问题。步骤:天然水→①沉降→②过滤→③曝气→④离子交换→⑤消毒→纯净水
(1)该地区的天然水属于???????????????????(“硬水”或“软水”)。
(2)在第①步中需要加入凝聚剂,常用的凝聚剂可以是??????????????????????。
(3)经过第④步离子交换后要经过杀菌消毒才能直接饮用。常用的消毒方式有???????。
(4)若采用药剂法软化天然水,可以向其中加入碳酸钠,发生反应的离子反应方程式是???
????????????????????????????,如果是暂时硬度,可用加热的方法除去,请写出发生的化学反应方程式????? ????????????????????????????????????????(写出一个即可)。
????????????????????????????????????????(写出一个即可)。
参考答案:
 本题解析:略
本题解析:略
本题难度:一般
2、填空题 (10分)亚氯酸钠(NaClO2)是一种重要的含氯消毒剂。以下是过氧化氢法生产亚氯酸钠的工艺流程图

已知:①NaClO2的溶解度随温度升高而增大,适当条件下可结晶析出NaClO2・3H2O。
②ClO2的沸点为283 K,纯ClO2易分解爆炸,常用稀有气体或空气稀释防止爆炸性分解
③HClO2在25 ℃时的电离常数与硫酸的第二步电离常数相当,可视为强酸。
(1)160 g/L NaOH溶液的物质的量浓度为____________________?。若要计算该溶液的质量分数,还需要的一个数据是__________________ 。
(2)ClO2发生器中所发生反应的离子方程式为__________________________
(3)吸收塔中为防止产生NaClO2被继续还原成NaCl,所用还原剂的还原性应适中。除H2O2处,还可以选择的还原剂是(????)(填序号)
A.Na2O2
B.Na2S
C.FeCl2
D.KMnO4
(4)写出吸收塔中发生反应的化学方程式____________________________
(5)从滤液中得到NaClO2・3H2O晶体还必须进行的操作是_____________ (填操作步骤)
参考答案:(10分)(1)4mol/L???溶液的密度
(2)2
本题解析:略
本题难度:一般
3、填空题 (12分)工业上生产高氯酸(沸点:90oC)时还同时生产了亚氯酸钠,其工艺流程如下:
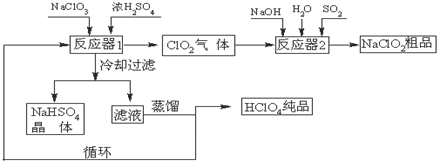
(1)冷却过滤的目的是降低NaHSO4的??????????并分离出NaHSO4晶体。
(2)反应器2中发生反应的离子方程式为??????????????????????????????????。SO2的作用是作??????剂。
(3)循环使用的物质是??????????????。
(4)可以通过蒸馏滤液的方法得到高氯酸的原因可能是????????????????????????????。
(5)工业上用铂作阳极、铜或银作阴极电解盐酸也可制得高氯酸,在阳极区可得到20%的高氯酸。写出阳极的电极反应式(其中盐酸与高氯酸以化学式出现)????????????????????????????。
参考答案:(12分)(1)溶解度(2分)(2)2ClO2+SO2+4O
本题解析:(1)溶解度?NaHSO4的溶解度随温度的升高而增大,随温度的降低而减小。冷却后更易析出NaHSO4晶体。
(2)2ClO2+SO2+4OH-=2ClO2-+SO42-+2H2O
在反应中由的SO2硫元素由+4价到+6价,失去电子,为还原剂
(4)蒸馏时,物质按沸点由低到高依次被蒸馏出。高氯酸的沸点为90 oC,很容易蒸出
(5)根据电解池原理,阳极物质失去电子,化合价升高,被氧化
本题难度:一般
4、选择题 下列说法错误的是( )。
A.对废旧金属的最好处理方法是回收、再利用
B.提炼金属要经过矿石的富集、冶炼、精炼三步
C.活泼金属的冶炼都是通过电解其盐溶液制得
D.热还原法中还原剂有焦炭、一氧化碳、氢气或活泼金属等
参考答案:C
本题解析:活泼金属的冶炼是通过电解其熔融状态的盐制得。故C项错误。
本题难度:一般
5、填空题 人们常用比喻的手法来描述材料的属性,比如“薄如纸,润如玉,声如磬,明如镜”是形容中国发明的 _____________;也可借用材料的属性来丰富比喻,比如借用铜、铁的坚硬,就有了“铜墙铁壁”这类词语。
参考答案:瓷器
本题解析:
本题难度:简单