微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 下列除杂方法正确的是
A.乙烷气体中混有乙烯,通入氢气,使乙烯发生加成反应
B.氯化钠溶液中混有少量硫酸钠,加入适量硝酸钡溶液,过滤
C.乙醇中混有乙酸,加入氢氧化钠后,分液
D.二氧化碳气体中混有少量的二氧化硫,通入酸性高锰酸钾溶液
参考答案:D
本题解析:略
本题难度:简单
2、实验题 (13分)(1)如图所示装置,为实现下列实验目的,其中y端适合于作入口的是_____多项)
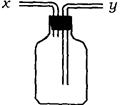
A 瓶内盛液体干燥剂,用以干燥气体
B 瓶内盛液体洗涤剂,用以除去某气体中的杂质
C 瓶内盛水,用以测量某难溶于水的气体的体积
D 瓶内贮存气体,加水时气体可被排出
E 收集密度比空气大的气体
F 收集密度比空气小的气体
(2) 浓H2SO4和木炭在加热时发生反应的化学方程式是_______________________。
图中虚线框中的装置可用来检验浓硫酸与木炭粉在加热条件下反应产生的所有气体产物,

填写下列空白。
①A中无水硫酸铜的作用_____________。
②证明SO2一定存在的现象是_____________。
③C中酸性KMnO4溶液的作用_____________。
④证明CO2一定存在的现象是_____________。
参考答案:(1)??? A B E??? (2) C+2H2SO4
本题解析:(1)由图可以看出y导管插入到试剂瓶的底部,因此可用来干燥某些气体,也可用来除去气体中的某些杂质,或者用来收集密度大于空气的某些气体。若瓶内盛水,用以测量某难溶于水的气体的体积,则进气口应是x导管。同样瓶内贮存难溶于水的气体,加水时气体可被排出,进气口同样应是x导管。收集密度比空气小的气体,进气口应是x导管。故正确的答案是A B E。
(2)浓硫酸具有强氧化性,在加热的条件下可氧化单质碳,方程式为C+2H2SO4 CO2↑+2SO2↑+2H2O。产物有三种水蒸气、CO2和SO2,验证水蒸气用无水硫酸铜,CO2用饱和石灰水,SO2用品红溶液。由于后两者都需要通过溶液,因此首先验证水蒸气。因为SO2也可以使石灰水变混浊,因此在检验CO2之前,需要先检验SO2,并且还要完全除去SO2,以避免干扰CO2的检验。
CO2↑+2SO2↑+2H2O。产物有三种水蒸气、CO2和SO2,验证水蒸气用无水硫酸铜,CO2用饱和石灰水,SO2用品红溶液。由于后两者都需要通过溶液,因此首先验证水蒸气。因为SO2也可以使石灰水变混浊,因此在检验CO2之前,需要先检验SO2,并且还要完全除去SO2,以避免干扰CO2的检验。
本题难度:一般
3、实验题 (10分)“酒是陈的香”,就是因为酒在储存过程中生成了有香味的乙酸乙酯,在实验室我们也可以用如右图所示的装置制取乙酸乙酯。完成下列问题:
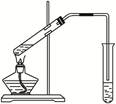
(1)写出制取乙酸乙酯的化学反应方程式__________________________________________。
(2)在大试管中配制一定比例的乙醇、乙酸和浓硫酸的混合液的方法是:________________。
(3)浓硫酸的作用是:①___________________________;②___________________________。
(4)饱和碳酸钠溶液的主要作用是
__________________________________________________。
(5)装置中通蒸气的导管要插在饱和碳酸钠溶液的液面上,不能插入溶液中,目的是防止
___________________________________________。
(6)若要把制得的乙酸乙酯分离出来,应采用的实验操作是____________________________。
(7)做此实验时,有时还向盛乙酸和乙醇的试管里加入几块碎瓷片,其目的是
______________________________________________________________________________。
(8)生成乙酸乙酯的反应是可逆反应,反应物不能完全变成生成物,反应一段时间后,就达到了该反应的限度,即达到化学平衡状态。下列描述能说明乙醇与乙酸的酯化反应已达到化学平衡状态的有(填序号) _________________。
①单位时间里,生成1 mol乙酸乙酯,同时生成1 mol水
②单位时间里,生成1 mol乙酸乙酯,同时生成1 mol乙酸
③单位时间里,消耗1 mol乙醇,同时消耗1 mol乙酸
④正反应的速率与逆反应的速率相等
⑤混合物中各物质的浓度不再变化
参考答案:
(1) 本题解析:该题是将乙酸乙酯的制取实验和无机化学的化学平衡有机结合起来的一道综合题。它涉及乙酸乙酯制取的各个环节,都是最基本的知识,而平衡状态的判断也是基础性的,根据平衡移动原理很容易进行判断。
本题解析:该题是将乙酸乙酯的制取实验和无机化学的化学平衡有机结合起来的一道综合题。它涉及乙酸乙酯制取的各个环节,都是最基本的知识,而平衡状态的判断也是基础性的,根据平衡移动原理很容易进行判断。
本题难度:简单
4、实验题 (9分)甲、乙、丙三位同学分别用如下三套实验装置及化学药品(其中碱石灰为固体氢氧化钠和生石灰的混合物)制取氨气。请你参与探究,并回答下列问题:
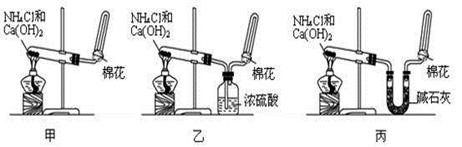
(1)三位同学制取氨气的化学方程式为: _____?????????__________________________。
(2)三位同学都用向下排空气法收集氨气,其原因是_______________________________.
(3)三位同学用上述装置制取氨气时,其中有一位同学没有收集到氨(如果他们的实验操作都正确),你认为没有收集到氨气的同学是___________填(“甲”、“乙”或“丙”),收集不到氨气的主要原因是_____________________________________(用化学方程式表示)。
(4 )检验氨气是否收集满的方法是(简述操作方法、现象和结
)检验氨气是否收集满的方法是(简述操作方法、现象和结 论)____________________
论)____________________
_____________________________________________________________________________。
(5)三位同学都认为他们的实验装置也可用于加热碳酸氢铵固体制取纯净的氨气,你判断能够达到实验目的的是___________(填“甲”、“乙”或“丙”),该装置中的NH4HCO3固体能否 用NH4Cl固体代替制NH3?______________(填“能”或“不能”)。
用NH4Cl固体代替制NH3?______________(填“能”或“不能”)。
参考答案:(1)2NH4Cl+Ca(OH)2=2NH3↑+2H2O+C
本题解析:略
本题难度:一般
5、填空题 哈伯因为氨气的合成曾获1918年诺贝尔奖。
(1)写出实验室由氯化铵和熟石灰加热制取氨气的化学方程式:???????????????????????。检验氨气已装满的方法是:用_____________试纸靠近集气瓶口,现象为_________________。
(2)用图装置进行喷泉实验, 若加入酚酞,得到红色喷泉,若要得到蓝色喷泉呢,应加入酸碱指示剂?????????。

(3)完成氨催化氧化生成为NO的反应方程式,4NH3+???O2="==4NO" + 6?????,产物NO能在通常状况下被空气氧化为NO2,请完成下列反应生成硝酸的化学方程式:
4NO+?O2+2H2O="==" 4HNO3
??NO2+??????O2 +?H2O="==" 4HNO3
(4)1.28 gCu与足量的浓硝酸反应生成的气体与一定量的O2混合,然后通入水中恰好完全反应无气体剩余,则该氧气的物质的量为??????mol.
参考答案:(1)2NH4Cl + Ca(OH)2 本题解析:
本题解析:
试题分析:(1)实验室由氯化铵和熟石灰加热制取氨气的化学方程式是2NH4Cl + Ca(OH)2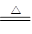 ?CaCl2 + 2NH3↑ + 2H2O。氨气是一种碱性气体,溶于水显碱性,所以可用用湿润的红色石蕊试纸靠近集气瓶口,而现象则是试纸变为蓝色。
?CaCl2 + 2NH3↑ + 2H2O。氨气是一种碱性气体,溶于水显碱性,所以可用用湿润的红色石蕊试纸靠近集气瓶口,而现象则是试纸变为蓝色。
(2)碱液能使紫色的石蕊试纸变为蓝色,所以若要得到蓝色喷泉呢,应加入酸碱指示剂石蕊试液。
(3)根据原子守恒可知,另外一种生成物应该是水。在反应中氮元素的化合价由-3价升高到+2价,失去5个电子,而氧元素的化合价从0价降低到-2价,得到2个电子,所以根据电子的得失守恒可知,配平后的方程式是4NH3+5O2="==4NO" + 6H2O;同样分析可知,另外两个反应的化学方程式分别是4NO+3O2+2H2O=4HNO3、4NO2+O2 +2H2O=4HNO3。
(4)浓硝酸的还原产物是NO2,和氧气混合溶于水后又生成硝酸,所以在反应中铜失去的电子相当于被氧气得到。所以根据电子的得失守恒可知,需要氧气的物质的量是 。
。
点评:该题是中等难度的试题,试题基础性强,难易适中,侧重对学生能力的培养和解题方法的指导与训练。有利于培养学生的逻辑推理能力和创新思维能力。氧化还原反应的有关配平和计算的关键是准确判断出有关元素的化合价变化情况,然后根据电子的得失守恒即可得出正确的结论。
本题难度:一般