微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 在酸性溶液中,能大量共存的离子组是(? )
A.Mg2+、Fe3+、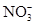 、SCN-
、SCN-
B.Al3+、Fe2+、Cl-、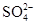
C.K+、Na+、Cl-、
D.Na+、Ba2+、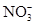 、
、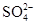
参考答案:B
本题解析:
试题分析:分析题中的指定条件,确定B项可大量共存。
本题难度:简单
2、选择题 某碱性溶液中,可以大量共存的离子组是( )
A.K+、Na+、HCO3-、NO3-
B.H+、Mg2+、SO42-、NO3-
C.Na+、SO42-、Cl-、ClO-
D.Ag+、K+、NO3-、Na+
参考答案:A、HCO3-与OH-反应生成CO32-和H2O而不能大量共
本题解析:
本题难度:一般
3、填空题 (12分)①、同温、同压下,质量相等的SO2和CO2相比较,体积之比为 ,已知SO2和CO2均为酸性氧化物,写出CO2与足量NaOH溶液反应的离子方程式 。
②、某溶液中可能含有大量下列阴离子:OH-、SO4 91Exam.org2-、CO32-、Cl-。
(1)当溶液中存在大量H+时,则溶液中不可能有 。
(2)当溶液中有大量的Ba2+存在时,则溶液中不可能有 ,用离子方程式写出不可能存在的原因 , 。
参考答案:(本题共12分)①11:16(2分)
本题解析:
试题分析:①二氧化硫的摩尔质量是64g/mol,二氧化碳的摩尔质量是44g/mol,所以同温同压下,质量相等的二者的体积比等于物质的量之比等于1/64:1/44=11:16;酸性氧化物与碱反应生成盐和水,二氧化碳与足量氢氧化钠反应生成碳酸钠和水,离子方程式为CO2+2OH-=CO32-+H2O;
②、(1)因为OH-、CO32-均与氢离子反应分别生成水、二氧化碳气体,所以当溶液中存在大量H+时,则溶液中不可能有CO32-、OH-;
(2)因为硫酸根离子、碳酸根离子均与钡离子反应生成沉淀,所以当溶液中有大量的Ba2+存在时,则溶液中不可能有SO42-、CO32-,反应的离子方程式是Ba2++ SO42- BaSO4↓、Ba2++ CO32-
BaSO4↓、Ba2++ CO32- BaCO3↓。
BaCO3↓。
考点:考查物质的量的有关计算,离子反应的判断与离子方程式的书写
本题难度:一般
4、选择题 在碱性溶液中能够大量共存且溶液为无色透明的离子组是( )
A.Na+NH4+NO3-Cl-
B.Na+K+CO32-NO3-
C.K+Ba2+HCO3-Cl-
D.Na+K+MnO4-SO42-
参考答案:碱性溶液中能够大量共存且溶液为无色透明,说明溶液中存在电离的
本题解析:
本题难度:一般
5、填空题 (12分)某中学化学兴趣小组为了调查当地某一湖泊的水质污染情况,在注入湖泊的3个主要
水源的入口处采集水样,并进行了分析,给出了如下实验信息:其中一处水源含有A、B两种物质,一处含有C、D两种物质,一处含有E物质,A、B、C、D、E为五种常见化合物,均由下表中的离子形成:
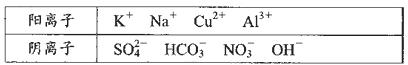
为了鉴别上述化台物。分别完成以下实验,其结果是:
①将它们溶于水后,D为蓝色溶液,其他均为无色溶液;
②将E溶液滴入到C溶液中出现白色沉淀,继续滴加,沉淀溶解;
③进行焰色反应,只有B、C为紫色(透过蓝色钻玻璃);
④在各溶液中加入硝酸锁溶液,再加过量稀硝酸,A中放出无色气体,C、D中都能产生白色沉淀:
⑤将B、D两溶液混合,未见沉淀或气体生成。
根据上述实验填空:
(1)写出B、D的化擎式:B________,D________。
(2)将含I mol A的溶液与含l molE的溶液反应后蒸于,仅得到一种化台物,该化合物的化学式为______。
(3)在A溶液中加入少量澄清石灰水,其离子方程式为________________。
(4)C常用作净水剂,用离子方程式和适当文字说明其净水原理_____________。
(5)若向含溶质lmol的C溶液中逐滴加入Ba(OH)2溶液,生成沉淀质量最大为______________g。
参考答案:(1)KNO3(2分) CuSO4(
本题解析:
试题分析:①将它们溶于水后,D为蓝色溶液,其他均为无色溶液,因此D中含有铜离子;②将E溶液滴入到C溶液中出现白色沉淀,继续滴加,沉淀溶解,白色沉淀应该是氢氧化铝,所以E是强碱,C中含有铝离子;③进行焰色反应,只有B、C为紫色(透过蓝色钻玻璃),所以E是氢氧化钠,B、C中含有钾离子;④在各溶液中加入硝酸锁溶液,再加过量稀硝酸,A中放出无色气体,因此A中含有碳酸氢根离子,则A是碳酸氢钠。C、D中都能产生白色沉淀,白色沉淀是硫酸钡,所以C是硫酸铝钾,D是硫酸铜:⑤将B、D两溶液混合,未见沉淀或气体生成,因此B是硝酸钾。
(1)根据以上分析可知出B、D的化学式分别为KNO3、CuSO4。
(2)1mol碳酸氢钠与1mol氢氧化钠反应生成1mol碳酸钠,因此蒸干得到的是碳酸钠,化学式为Na2CO3。
(3)碳酸氢钠溶液与少量澄清石灰水反应生成碳酸钙、碳酸钠和水,其离子方程式为2HCO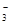 + Ca2+ +2OH-=CaCO3↓ + CO
+ Ca2+ +2OH-=CaCO3↓ + CO + H2O。
+ H2O。
(4)硫酸铝钾溶于水电离出的铝离子水解生成氢氧化铝胶体,Al3+ + 3H2O Al(OH)3(胶体)+3H+,水解生成的氢氧化铝胶体能吸附水中的悬浮物净水。
Al(OH)3(胶体)+3H+,水解生成的氢氧化铝胶体能吸附水中的悬浮物净水。
(5)向含溶质lmol的硫酸铝钾溶液中逐滴加入Ba(OH)2溶液,当钡离子完全转化为硫酸钡沉淀使,沉淀质量最大,其质量为2mol×233g/mol=466g。
考点:考查离子共存、离子检验以及离子反应的有关判断与计算
本题难度:困难