参考答案:
物质
粒子数(个)
质量(g)
物
本题解析:
试题分析:氩气的物质的量为0.2mol,粒子数=6.02×1023×0.2=1.204×1023,质量m=0.2×4=0.8g,摩尔质量为4g/mol;S的粒子数为1.204×1023,即S的物质的量为1.204×1023/6.02×1023=0.2,质量m=0.2×32=6.4g,摩尔质量为32g/mol;CO2的质量为22g,n=22/44=0.5mol,所以粒子数=6.02×1023×0.5=3.01×1023,摩尔质量为44g/mol;C12H22O11的物质的量为0.25mol,粒子数=6.02×1023×0.25=1.505×1023,质量m=0.25×342=85.5g,摩尔质量为342g/mol。
考点:阿伏加德罗常数、物质的量
点评:该题以表格的形式,已知其中的某个量,然后根据这个量来计算其他的量,该题涉及的计算比较简单,但是要注意运算的正确性。
本题难度:一般
2、选择题 1?mol・L-1H2SO4溶液的含义是[???? ]
A.1?L水中含有1?mol?H2SO4
B.1?L溶液中含有1?mol?H+
C.将98?g?H2SO4溶于1?L水中配成溶液
D.1?L?H2SO4溶液中含98?g?H2SO4
参考答案:D
本题解析:
本题难度:简单
3、填空题 (1)1L?Na2SO4?溶液中,如果含钠元素的质量是2.3g,溶液中?SO42-物质的量浓度为______?mol/L.
(2)如果实验室没有?Na2SO4,可用?NaOH?和?H2SO4?反应配制?Na2SO4?溶液,从理论上计算,配制符合(1)的要求的?Na2SO4?溶液,需要NaOH的质量为______g?和?1.0mol/L硫酸溶液的体积为______?mL.(说明:按计算用量混合后,用蒸馏水稀释至1L?即可)
参考答案:(1)钠离子的物质的量=
本题解析:
本题难度:一般
4、选择题 设NA表示阿伏加德罗常数,下列叙述不正确的是????????(???)
A.常温常压下,NA个CO2分子的质量总和为44 g
B.常温常压下,1mol氦气含有的氦原子为1 NA
C.12.4 g 白磷(P4)中含有的磷原子数为0.4 NA
D.0.1 mol・L-1稀硫酸100 mL中含硫酸根个数为0.1 NA
参考答案:D
本题解析:
试题分析:A、NA个CO2分子的物质的量为1mol,故其质量为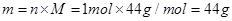 。 。
B、氦气的化学式为Ne,为单原子分子。故1mol氦气所含有的氦原子为1NA。
C、12.4 g 白磷(P4)的物质的量为 本题难度:一般 本题难度:一般
5、填空题 实验室用Na2SO4?10H2O配制500ml,0.100mol/L的Na2SO4溶液
(1)所需主要仪器为:药匙、托盘天平、烧杯、胶头滴管、______、______.
(2)本实验须称量硫酸钠晶体(Na2SO4?10H2O)为______g.
(3)用Na2SO4?10H2O配制标准溶液的正确顺序是______.
A.冷却??B.称量??C.洗涤??D.定容??E.溶解??F.摇匀??G.移液
(4)配制过程中出现以下情况,对所配溶液浓度有何影响(填“偏高”“偏低”“不变”)
①没有洗涤烧杯和玻璃棒.______.
②定容时俯视容量瓶的刻度线.______.
参考答案:(1)根据实验操作的步骤有计算、称量、溶解、冷却、移液、洗涤
本题解析:
本题难度:一般
|