微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 常温下,下列各组离子在指定溶液中定能大量共存的是( )
A.水电离的H+浓度为1×10-10mol/L,的溶液中:Al02-、SiO32-、K+、Na+
B.Kw/c(H+)=0.lmol/L的溶液中:Na+、SiO32-、I-、CO32-
C.pH=l的溶液中:NH4+、Na+、SO42-、C17H35COO-
D.0.lmol/L的NaHSO4溶液中K+、Fe2+、Cl-、NO3-
参考答案:A.水电离的H+浓度为1×10-10mol/L,为酸或碱溶液
本题解析:
本题难度:一般
2、选择题 在pH=1的溶液中,可以大量共存的离子是
A.K+、Na+、SO42-、SO32-
B.NH4+、Mg2+、SO42-、Cl-
C.Na+、K+、HCO3-、Cl-
D.K+、Na+、ClO-、NO3-
参考答案:B
本题解析:
试题分析:pH=1的溶液是酸性溶液,含有大量的氢离子。A、氢离子与SO32-反应生成二氧化硫和水,不能大量共存,错误;B、四种离子与氢离子都不反应,且彼此也不反应,可以大量共存,正确;C、氢离子与碳酸氢根离子反应生成二氧化碳,不能大量共存,错误;D、氢离子与次氯酸根离子反应生成弱电解质次氯酸,不能大量共存,错误,答案选B。
考点:考查酸性条件下离子大量共存的判断
本题难度:一般
3、计算题 Ⅰ.某溶液中仅含下表离子中的5种离子(不考虑水的电离及离子的水解),且离子的物质的量均为1mol。
阴离子
| SO42-、NO3-、Cl-
|
阳离子
| Fe3+、Fe2+、NH4+、Cu2+、Al3+
?
①若向原溶液中加入KSCN溶液,无明显变化。②若向原溶液中加入过量的盐酸,有气体生成,溶液中阴离子种类不变。③若向原溶液中加入BaCl2溶液,有白色沉淀生成。试回答下列问题
(1)若先向原溶液中加入过量的盐酸,再加入KSCN溶液,现象是????????????。
(2)原溶液中含有的阳离子是???????????????。
(3)向原溶液中加入足量的盐酸,发生反应的离子方程式为??????????????????。
(4)向原溶液中加入足量的NaOH溶液,充分反应后,过滤、洗涤、灼烧,最终所得固体用托盘天平称量质量为????????????。
Ⅱ. 草酸亚铁晶体(FeC2O4・2H2O)、碳酸锂和二氧化硅在氩气中高温反应可制备锂电池的正极材料硅酸亚铁锂(Li2FeSiO4)。草酸亚铁晶体在氩气气氛中进行热重分析,结果如右图所示(TG%表示残留固体质量占原样品总质量的百分数),请回答下列问题:
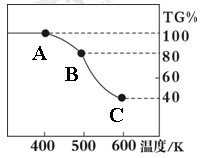
(5)草酸亚铁晶体中碳元素的化合价为:?????????????
(6)A→B发生反应的化学方程式为???????????????????。
(7)精确研究表明,B→C实际是分两步进行的,每一步只释放一种气体,第二步释放的气体的相对分子质量较第一步的大,则第一步释放的气体化学式为:?????????;释放第二种气体时,反应的化学方程式为???????????????????????????????。
参考答案:(16分,每空2分)(1)溶液呈红色(2分)????(2)F
本题解析:
试题分析:Ⅰ.若向溶液中加入KSCN溶液,无明显变化,说明原溶液中不含Fe3+;若向溶液中加入过量的盐酸,有气体生成,溶液中阴离子种类不变,说明原溶液中含有Cl-,该气体只能是NO,说明含有具有氧化性的NO3-和具有还原性的Fe2+。若向溶液中加入BaCl2溶液,有白色沉淀生成,说明原溶液中含有SO42-。各离子的物质的量均为1mol,因此根据电荷守恒可知还应含有Cu2+,所以原溶液中所含阳离子是Fe2+、Cu2+,阴离子是NO3-、Cl-、SO42-。
(1)如果先加入盐酸,在酸性条件下N
本题难度:困难
4、实验题 (18分)以铝灰(主要成分为Al、Al2O3,另有少量CuO、SiO2、FeO和Fe2O3杂质)为原料,可制得液体聚合氯化铝 [Alm(OH)nCl3m―n],生产的部分过程如下图所示(部分产物和操作已略去)。
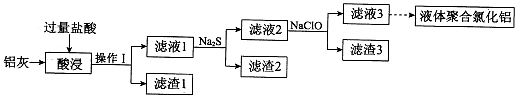
(1)Al2O3与盐酸反应的离子方程式是_____________________。
(2)滤渣I是__________。滤渣2为黑色,该黑色物质的化学式是___________。
(3)向滤液2中加入NaClO溶液至不再产生红褐色沉淀,此时溶液的pH约为3.7。其中NaClO的作用是___________。该过程发生反应的离子方程式为______________。
(4)将滤液3的pH调至4.2~4.5,利用水解反应得到液体聚合氯化铝。该反应的化学方程式为_____________________。
(5)Na2S溶液呈碱性的原因是________(用离子方程式表示)。该溶液中c(Na+)=________。
参考答案:(1)Al2O3+6H+ =2 Al3++3H2O
(
本题解析:
试题分析:分析题给信息和流程知,铝灰加过量盐酸酸浸发生的反应为2Al+6H+ =2Al3++3H2、Al2O3+6H+ =2Al3++3H2O、CuO+2H+==Cu2+ +H2O、FeO+2H+==Fe2+ +H2O、Fe 2O3 + 6H+="=2" Fe 3+ + 3H2O,经操作Ⅰ过滤得滤渣1为SiO2,滤液1为氯化铝、氯化铁、氯化铜、氯化亚铁和盐酸的混合液,向其中加入硫化钠生成黑色氯化铜沉淀,过滤得滤渣2为硫化铜,滤液2为氯化铝、氯化铁和氯化亚铁的混合液,向其中加入次氯酸钠,将Fe2+氧化为Fe3+,使Fe3+转化为Fe(OH)3,滤液3可制得液体聚合氯化铝[Alm(OH)nCl3m―n]。(1)Al2O3与盐酸反应生成氯化铝和水,离子方程式是Al2O3+6H+ =2 Al3++3H2O ;(2)滤渣I是SiO2,滤渣2为黑色,该黑色物质的化学式是CuS;(3)向滤液2中加入NaClO溶液至不再产生红褐色沉淀,此时溶液的pH约为3.7。 其中NaClO的作用是将Fe2+氧化为Fe3+,使Fe3+转化为Fe(OH)3 。该过程发生反应的离子方程式为2Fe2++ClO―+2H+=2Fe3++Cl―+H2O、Fe3++3ClO―+3H2O=Fe(OH)3↓+3HClO;(4)将滤液3的pH调至4.2~4.5,利用水解反应得到液体聚合氯化铝。该反应的化学方程式为mAlCl3+nH2O = Alm(OH)nCl3m-n+nHCl;(5)硫化钠为强碱弱酸盐,硫离子分步水解,以第一步水解为主,Na2S溶液呈碱性的原因是S2―+H2O HS―+OH―。该溶液中根据物料守恒有c(Na+)=2c(S2―)+2c(HS―)+2c(H2S),根据电荷守恒有2c(S2―)+c(HS―)+c(OH―)-c(H+)。 HS―+OH―。该溶液中根据物料守恒有c(Na+)=2c(S2―)+2c(HS―)+2c(H2S),根据电荷守恒有2c(S2―)+c(HS―)+c(OH―)-c(H+)。
考点:以液体聚合氯化铝的化工生产流程为载体考查物质的分离、提纯,化学方程式、离子方程式的书写及盐类水解原理的应用。
本题难度:困难
5、填空题 (16分)某强酸性溶液X,含Ag+、Al3+、SiO2-3、NH+4、Fe2+、Fe3+、CO2-3、Cl-、NO-3中的一种 或几种离子,取X溶液进行连续实验,能实现如下转化:
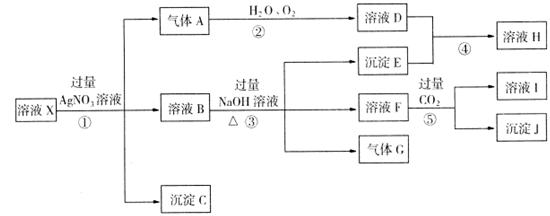
依据以上信息,回答下列问题:
(1)上述离子中,溶液x中肯定含有的是: ;不能肯定的是: ;对不能确定是否存在的离子,可以另取x溶液于一支试管中,选择下列试剂中的某一种加入X溶液,根据现象就可判断,则试剂可以选(若多种选法中间加“或"字间隔): 。
①酚酞试剂,②石蕊试剂,③pH试纸,④KSCN溶液,⑤KMnO4溶液,⑥苯酚溶液
(2)气体G的化学式为: ;沉淀E的化学式为: ;沉淀J的化学式为: 。
(3)实验中,产生的气体A为无色,但如果暴露在空气中可以观察到的现象是: ;写出步骤①中生成气体A的离子方程式 。
(4)要使步骤②中,A、H2O、O2三种物质恰好发生化合反应,则A、H2 O、O2物质的量之比是: 。
参考答案:(16分)
 本题解析:略 本题解析:略
本题难度:一般
|