微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 下列离子方程式书写正确的是( )
A.用NaOH溶液吸收氯气:2OH-+Cl2 =Cl-+ClO-+H2O
B.用小苏打治疗胃酸过多: CO32-+2H+=CO2↑+H2O
C.Fe(OH)3溶于氢碘酸中:Fe(OH)3 + 3H+ =Fe3+ + 3H2O
D.用氨水吸收足量的SO2气体:OH-+SO2 = HSO3-
参考答案:A
本题解析:
试题分析:小苏打是碳酸氢钠,B不正确;铁离子具有氧化性,碘离子具有还原性,C不正确,反应中生成单质碘、碘化亚铁和水;氨水是弱碱,应该有化学式表示,D不正确,答案选A。
点评:该题是高考中的高频题,属于中等难度的试题,试题侧重考查学生的能力,有助于培养学生的应试能力。该题需要明确判断离子方程式正确与否的方法一般,即(1)检查反应能否发生。(2)检查反应物、生成物是否正确。(3)检查各物质拆分是否正确。(4)检查是否符合守恒关系(如:质量守恒和电荷守恒等)。(5)检查是否符合原化学方程式。
本题难度:简单
2、选择题 向明矾溶液中逐渐滴加Ba(OH)2溶液,符合要求的离子方程式为
A.加入过量的Ba(OH)2溶液时:2Al3++3SO42-+3Ba2++6OH―→ 2Al(OH)3↓+3BaSO4↓
B.溶液恰好呈中性时:2Al3++3SO42-+3Ba2++6OH―→ 2Al(OH)3↓+3BaSO4↓
C.SO42-离子恰好完全沉淀时:Al3++2SO42-+2Ba2++4OH―→ AlO2-+2BaSO4↓+2H2O
D.明矾与Ba(OH)2按物质的量比1∶1反应时:
Al3++SO42-+Ba2++3OH―→ Al(OH)3↓+BaSO4↓
参考答案:BC
本题解析:
正确答案:BC
A、加入过量的Ba(OH)2溶液时:Al3++2SO42-+2Ba2++4OH―= AlO2-+2BaSO4↓+2H2O
D、2Al3++3SO42-+3Ba2++6OH―="2" Al(OH)3↓+3BaSO4↓
本题难度:简单
3、选择题 下列离子方程式书写正确的是
A.NaHSO4溶液与Ba(OH)2溶液反应至中性:H++SO42―+Ba2++OH― = BaSO4↓+H2O
B.酸性条件下KIO3溶液与KI溶液发生反应生成I2: IO3-+5I-+3H2O=3I2+6OH-
C.NH4HCO3溶液与足量浓NaOH溶液反应: NH4+ +HCO3- + 2OH-= NH3↑ +2H2O+CO32-
D.氯气和水的反应: C12+H2O=2H++C1-+ClO-
参考答案:C
本题解析:A不正确,至中性时,方程式为2NaHSO4+Ba(OH)2=BaSO4+2H2O+Na2SO4。酸性条件下不可能生成OH-,应该是水,B不正确。次氯酸是弱电解质,用化学式表示,D是不正确。所以正确的答案是C。
本题难度:一般
4、选择题 下列表示正确的是?????
A.电解饱和氯化镁溶液的离子方程式是2Cl-+2H2O  H2↑+Cl2↑+2OH-
H2↑+Cl2↑+2OH-
B.工业制硫酸过程中,沸腾炉里的反应方程式是2S+3O2  2SO3
2SO3
C.泡沫灭火器的化学反应原理可表示为Al3++3HCO3-=Al(OH)3↓+3 CO2↑
D.表示硫酸与氢氧化钠溶液反应的中和热的热化学反应方程式是
H2SO4(aq)+2NaOH(aq)=Na2SO4(aq)+2H2O(l);△H="-57.3" kJ/mol
参考答案:C
本题解析:A错,电解饱和氯化镁溶液是Mg2++2Cl-+2H2O ? ??H2↑+Cl2↑+Mg(OH)2↓
??H2↑+Cl2↑+Mg(OH)2↓
B错,工业制硫酸过程中,沸腾炉里的反应方程式是:4FeS2 + 11O2=====
5、填空题 NH4Al(SO4)2是食品加工中最为快捷的食品添加剂,用于焙烤食品,工业上常用铝土矿(主要成分为Al2O3)来生产铵明矾NH4Al(SO4)2?12H2O,其工艺流程图如下
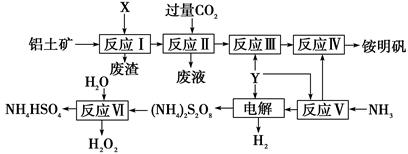
(1)流程图中X的电子式??????????????, Y为????????????(填化学式)溶液
(2)反应Ⅱ的离子方程式为????????????????????????????????????
(3)流程中可以循环使用的物质的名称是?????????????????????????
(4)反应Ⅵ的化学方程式为??????????????????????????????????????????
(5)对铵明矾NH4Al(SO4)2・12H2O高温分解的气体产物的预测不合理的是????????。
A.NH3、N2、SO2、H2O????? B.NH3、SO3、H2O
C.NH3、SO2、H2O????????? D.NH3、N2、SO3、SO2、H2O
(6)若同时制取铵明矾和硫酸铝,通过控制硫酸的用量调节两种产品的产量。若欲使制得的铵明矾和硫酸铝的物质的量之比为1:1,则投料时铝土矿中Al2O3和H2SO4的物质的量之比为____。
(7)向硫酸铝铵溶液中逐滴加入氢氧化钡溶液,不可能发生的反应是
A.4NH4Al(SO4)2+3Ba(OH)2=2(NH4)2SO4+3BaSO4↓+ Al2 (SO4)3+2Al(OH)3↓
B.2NH4Al(SO4)2+4Ba(OH)2=(NH4)2SO4+3BaSO4↓+Ba(AlO2)2
C.2NH4Al(SO4)2+3Ba(OH)2=(NH4)2SO4+3BaSO4↓+2Al(OH)3↓
D.NH4Al(SO4)2+2Ba(OH)2=NH3・H2O+2BaSO4↓+ Al(OH)3↓
参考答案:(1) 本题解析:
本题解析:
试题分析:铝土矿的主要成分是氧化铝,与X反应后的溶液与二氧化碳反应,故X为氢氧化钠溶液,反应后生成的偏铝酸钠溶液可以和过量的二氧化碳反应生成氢氧化铝沉淀和碳酸氢钠溶液,故X为氢氧化钠;反应Ⅲ为氢氧化铝中加上Y可以制得NH4Al(SO4)2,需要有氢离子溶解氢氧化铝,还有硫酸根离子,故Y为H2SO4;(2)反应II为偏铝酸钠溶液和二氧化碳的反应;(3)由工艺流程转化可知,Y为H2SO4,反应Ⅴ生成NH4HSO4,反应Ⅳ中NH4HSO4转化为铵明矾,反应Ⅵ也产生NH4HSO4,可见NH4HSO4可以在
本题难度:一般