��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1��ѡ���� ���и�������һ���ܴ����������??????????
A.�ں�����Fe3+����Һ�У�NH4+��Na+��Cl-��SCN-
B.��ǿ������Һ�У�Na+��K+��Al(OH)4-��CO32-
C.�ڼ�����Һ�У�NH4+��Al3+��SO42-��NO3-
D.��������pH=1����Һ�У�K+��Fe2+��Cl-��NO3-
�ο��𰸣�B
������������������A��Fe3+��SCN-���ܴ������棬C�������Һ��NH4+��Al3+���ܴ������棬D����������Һ��Fe2+��NO3-���ܴ������档��ѡB��
���㣺���ӹ���
���������Ӳ��ܴ��������һ������ǣ���1���ܷ������ֽⷴӦ������֮�䣨�����ɳ��������壬ˮ�����ᡢ������ѵ������ʣ�����2�������������������֮�䣨�磺Ca2+�� SO42-��Ag+�� SO42-������3������ȫˮ�������֮�䣬���Ԫ����������ε����������ӣ��磺Al3+�� Fe3+�� CO32-��HCO3-��AlO2-��ClO-��S2-�ȣ�����4���ܷ���������ԭ��Ӧ������֮�䣨�磺Fe ��H+��NO3-��S2-��ClO-��S2-�� Fe3+�ȣ�����5���ܷ�����Ϸ�Ӧ������֮�䣨�� Fe3+�� SCN-����������ӹ�������ʱ��Ӧ��ע����Ŀ����������������Ŀ������������һ���У�1����Һ������ԣ��ݴ����ж���Һ���Ƿ��д����� H+��OH-����2����Һ����ɫ������ɫʱ���ų� Cu2+�� Fe2+��Fe3+��MnO4-����ɫ���ӵĴ��ڣ���3����Һ�ľ��巴Ӧ�������硰������ԭ��Ӧ�������������۲�������������4���ǡ����ܡ����棬���ǡ�һ��������ȡ�
�����Ѷȣ�һ��
2��ѡ���� ��ɫ����Һ���ܴ����������������
A.HCO3-��Na+��K+��H+
B.Fe3+��H+��Na+��Cl-
C.I-��ClO-��K+��H+
D.Na+��Cl-��NO3-��CO32-
�ο��𰸣�D
�����������������������֮�䲻�ܽ������ˮ�����塢���������ܷ���������ԭ��Ӧ�����������ӵĹ������⣬��ע��Fe3+��ˮ��ҺΪ��ɫ�����
���A����HCO3-��H+�ܽ������ˮ�Ͷ�����̼���壬���ܴ������棬��A����
B����Fe3+��ˮ��ҺΪ��ɫ������ɫ��Һ��������B����
C����I-��ClO-��H+�ܷ���������ԭ��Ӧ�������Ӳ��ܴ������棬��C����
D����������֮�䲻��Ӧ������ˮ�о�Ϊ��ɫ�����ܹ��������棬��D��ȷ��
��ѡD��
���������⿼�����ӵĹ��棬��Ϥ����֮��ķ�Ӧ�ǽ����Ĺؼ���ע�����ø��ֽⷴӦ��������������ԭ��Ӧ�����ӵ���ɫ��֪ʶ����ɣ��ѶȲ���
�����Ѷȣ�һ��
3��ѡ���� ���з�Ӧ�в�����ȡ����Ӧ����
A.�ױ������ᡢŨ���Ṳ��
B.�ױ��ڹ�����������������Ӧ
C.���������ڴ��������¹������ɻ�����
D.����Һ���Ϻ��������������屽
�ο��𰸣�C
���������
�����Ѷȣ�����
4��ѡ���� ��MgSO4��Al2(SO4)3�Ļ����Һ�У���μ���NaOH��Һ������ͼ���У�����ȷ��ʾ������Ӧ����(�������ʾ����NaOH��Һ��������������ʾ��Ӧ���ɳ���������) [???? ]
A��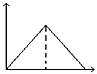
B��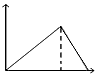
C��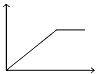
D��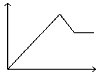
�ο��𰸣�D
���������
�����Ѷȣ�һ��
5��ѡ���� ��֪��HCO3��+AlO2��+H2O=Al(OH)3��+CO32��ij��Һ�п��ܺ���OH?��CO32?��AlO2?��SiO32?��SO42?��K+��Na+��Fe3+��Mg2+��Al3+�����ӣ�������Һ����μ���һ�����ʵ���������ʱ�����ɳ������ʵ����������������Ĺ�ϵ��ͼ��ʾ������˵���в���ȷ����
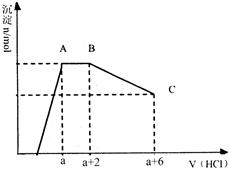
A��ԭ��Һ�϶�����OH?��CO32?��AlO2?��SiO32?
B��K+��Na+���ٺ�������һ��
C��n��C O32?����n��AlO2?��=3��2
D��aֵ�϶�����4/3
�ο��𰸣�C
�������������ͼ���֪�����û�г�����˵��һ������OH?����һ��û��Fe3+��Mg2+��Al3+������K+��Na+���ٺ�������һ�֡������ﵽ��ߺ��ּ��٣���˵��һ�����������������������˱��뺬��AlO2?�� SiO32?������AB��ȷ��A��B�Ǻ�CO32?������������2�����B��C���ܽ���������������������6���������n��CO32?����n��AlO2?����1�U2��C����ȷ�������ܽ�����������������6���������������������������2���������D��ȷ����ѡC��
�����Ѷȣ�һ��