微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、填空题 19世纪中叶,门捷列夫总结出了如下表所示的元素化学性质的变化规律。请回答
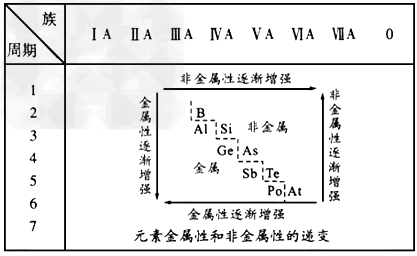
(1)门捷列夫的突出贡献是_______。 ????
A.提出了原子学说????B.提出分子学说 ????C.发现元素周期律????D.发现能量守恒定律
(2)该表变化表明_______。 ????
A.物质的性质总是在不断变化的 ????
B.元素周期表中最右上角的氦元素是非金属性最强的元素 ????
C.第IA族元素的金属性肯定比同周期的第ⅡA族元素的金属性强 ????
D.物质发生量变到一定程度必然引起质变 ????
(3)按照表中元素的位置,认真观察从第ⅢA族的硼到第ⅦA族的砹连接的一条折线,我们能从分界线附近找到_______。 ????
A.耐高温材料????B.新型农药材料 ????C.半导体材料????D.新型催化剂材料 ????
(4)据报道,美国科学家制得一种新原子283116X,它属于一种新元素116号元素(元素符号暂用X代替),关于它的推测正确的是_______。 ????
A.这种原子的中子数为167 ????B.它位予元素周期表中第六周期 ????
C.这种元素一定是金属元素 ????D.这种元素的原子易与氢化合
参考答案:(1)C?
(2)D?
(3)C?
(4)
本题解析:
本题难度:一般
2、选择题 下列说法正确的是
A.元素周期表包括7个横行、16个纵行
B.非金属性最强的元素是氟元素
C.氧元素位于第2周期Ⅵ族
D.钠的金属性比钾强
参考答案:B
本题解析:元素周期表包括7个横行(7个周期)、18个纵行(16个族);氧元素位于第2周期ⅥA族:同主族元素由上到下金属性增强.
本题难度:一般
3、选择题 下列说法正确的是
A.Li、Na、K原子的电子层数依次增多,最高正价依次升高
B.Si、P、S、Cl的原子序数依次增大,最低负价依次降低
C.Li、Be、B、C的最外层电子数依次增多,最高正价依次升高
D.所有的元素都有0价和负价,但是不一定有正价
参考答案:C
本题解析:逐项分析.
A.错误.Li、Na、K原子的电子层数分别为2、3、4,电子层数依次增多是正确的;但它们的最外层电子数都为1,最高正价都为+1,最高正价依次升高是错误的.
B.错误.Si、P、S、Cl的原子序数分别为4、5、6、7,原子序数依次增大是正确的;但其最低负价分别为-4、-3、-2、-1,-4<-3<-2<-1,由-4到-1化合价逐渐升高,最低负价依次降低是错误的.
C.正确.Li、Be、B、C的最外层电子数分别为1、2、3、4,最外层电子数依次增多是正确的,它们的最高正价分别为+1、+2、+3、+4,最高正价依次升高也是正确的.
D.错误.所有的元素都有0价,但是不一定有正价(如F元素);金属没有负价,故所有的元素都有负价是错误的.
本题难度:困难
4、选择题 下列元素中金属性最强的是( )
A.Na
B.K
C.Al
D.Si
参考答案:因Na、Al、Si均在第三周期,且原子序数依次增大,由同周期
本题解析:
本题难度:一般
5、选择题 温超导体中,铊(Tl)是其中成分之一,已知铊是铝的同族元素,关于铊的下列性质判断中可能错误的是
A.是银白色质软的金属
B.形成+3价的化合物
C.Tl(OH)3是两性氢氧化物
D.单质铊的还原性比单质铝强
参考答案:C
本题解析:
本题难度:简单